题目内容
9.由Cu(OH)2和CuO组成的混合物,测得其中含铜元素的质量分数为72%.取该混合物10g投入80g一定质量分数稀硫酸中恰好完全反应,所得溶液中溶质的质量分数为( )| A. | 20% | B. | 30% | C. | 36% | D. | 48% |
分析 根据铜元素的质量分数可计算铜元素的质量,利用反应后的溶质为硫酸铜,根据铜原子守恒来计算硫酸铜的质量,混合物与酸的质量和为溶液质量,最后计算溶质的质量分数.
解答 解:混合物中铜元素的质量为10g×72%=7.2g,
设恰好完全反应后溶液中硫酸铜的质量为x,
Cu(OH)2+H2SO4=CuSO4+2H2O;CuO+H2SO4=CuSO4+H2O;
由铜元素守恒可知,
Cu~CuSO4
64 160
7.2g x
$\frac{64}{7.2g}=\frac{160}{x}$
解得x=18g,
反应后溶液质量为10g+80g=90g,
则溶液中溶质的质量分数为:$\frac{18g}{90g}$×100%=20%,
故选:A.
点评 本题考查溶液中溶质质量分数的计算,学生应能利用元素守恒的方法来计算溶质的质量是解答中的关键,不可盲目利用化学方程式来计算溶质质量.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
20.下列说法正确的是( )
| A. | 稀盐酸可以去除氢氧化钠中的杂质碳酸钠 | |
| B. | 用燃烧的方法可以区别涤纶和腈纶 | |
| C. | 在化学反应中反应物相同,生成物可能不同 | |
| D. | 洗洁精可以溶解衣服上的油污 |
14.物质X )和物质Y
)和物质Y )的反应如图所示,对该反应的描述,下列反应方程式正确的是( )
)的反应如图所示,对该反应的描述,下列反应方程式正确的是( )
 )和物质Y
)和物质Y )的反应如图所示,对该反应的描述,下列反应方程式正确的是( )
)的反应如图所示,对该反应的描述,下列反应方程式正确的是( )
| A. | 3X+8Y═X3Y8 | B. | 3X+8Y═3XY2+2Y | C. | 3X+6Y═3XY2 | D. | X+2Y═XY2 |
18.下列与其它三种不同的是( )
| A. | 粮食发酵制成酒 | B. | 冰融化成水 | C. | 湿衣服晒干 | D. | 铁铸成锅 |




 已知①二氧化硫能使品红试液(一种红色溶液)褪色,二氧化碳不能,②Ca(OH)2+SO2═CaSO3(白色)↓+H2O,③二氧化硫能被高锰酸钾溶液吸收而二氧化碳不能,④木炭与浓硫酸在加热条件下发生反应生成二氧化硫、二氧化碳和水.
已知①二氧化硫能使品红试液(一种红色溶液)褪色,二氧化碳不能,②Ca(OH)2+SO2═CaSO3(白色)↓+H2O,③二氧化硫能被高锰酸钾溶液吸收而二氧化碳不能,④木炭与浓硫酸在加热条件下发生反应生成二氧化硫、二氧化碳和水.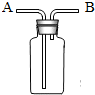 如图装置的用途多种多样,有“万能瓶”之称. 按下列要求回答问题:
如图装置的用途多种多样,有“万能瓶”之称. 按下列要求回答问题: