题目内容
1.某化工厂打算用 铜、硫酸和硝酸等原料制备Cu(NO3)2溶液,某同学通过查阅 资料设计出4种制备方案,其原理分别是:(假设原料利用率为100%)①Cu+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cu(NO3)2+2NO2↑+2H2O
②3Cu+8HNO3(稀)$\frac{\underline{\;\;△\;\;}}{\;}$3Cu(NO3)2+2NO↑+4H2O
③2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO; CuO+2HNO3═Cu(NO3)2+H2O
④Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O; CuSO4+Ba(NO3)2═Cu(NO3)2+BaSO4↓
(1)在①②③方案中,欲制取相同质量Cu(NO3)2,消耗的硝酸质量由多到少的顺序是①>②>③(填序号).
(2)在方案④中选用氢氧化钠溶液吸收产生的酸性气体的,该反应的化学方程式为2NaOH+SO2=Na2SO3+H2O.
(3)若在方案④中最后得到硫酸钡沉淀11.65克,则消耗的铜的质量为多少?
(列式计算,相对原子质量:H-l; N-14; S-32; O-16; Cu-64;Ba-137)
分析 根据反应的化学方程式可以判断欲制取相同质量Cu(NO3)2,消耗的硝酸质量由多到少的顺序;
氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)当制取硝酸铜的量是3Cu(NO3)2时,①消耗12HNO3,②消耗8HNO3,③消耗6HNO3.
故填:①>②>③.
(2)二氧化硫属于酸性气体,和氢氧化钠负硬度化学方程式为:2NaOH+SO2=Na2SO3+H2O.
故填:2NaOH+SO2=Na2SO3+H2O.
(3)解:设消耗铜的质量为x,
由Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O和CuSO4+Ba(NO3)2═Cu(NO3)2+BaSO4↓可知,Cu~BaSO4↓,
Cu~BaSO4↓,
64 233
x 11.65g
$\frac{64}{x}$=$\frac{233}{11.65g}$,
x=3.2g,
答:若在方案④中最后得到硫酸钡沉淀11.65克,则消耗的铜的质量为3.2g.
点评 计算消耗铜的质量时,可以根据铜和硫酸钡的质量关系进行计算,这样比较简单,要注意掌握这种方法.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
11.下列问题的研究中,没有利用对比实验思想方法且结论正确的是( )
| A. |  二氧化锰可以增加产生氧气的总量 | |
| B. |  水由氢元素和氧元素组成 | |
| C. |  燃烧需要与氧气接触、且温度达到着火点 | |
| D. |  二氧化碳能使石蕊变红 |
12.准确量取25毫升液体,一般应使用的仪器是( )
| A. | 10毫升量筒 | B. | 100毫升烧杯 | C. | 50毫升烧杯 | D. | 50毫升量筒 |
6.小红学习了元素周期表的相关知识后,对教材中“元素周期表也可以竖着(按族)读,每一竖列中元素的化学性质都很相似”这个说法产生了兴趣,她和同学们进行如下探究:
【提出问题】查阅元素周期表后发现钙元素和镁元素同在一个竖列里,她已经知道氢氧化钙溶液能使酚酞试液变红,她通过实验来探究不溶性的氢氧化镁是否也能使酚酞试液变红:将适量氢氧化镁分别加入到盛有冷水和热水的烧杯中,搅拌并分别向两烧杯中滴加酚酞试液,发现盛冷水的烧杯中酚酞试液没有变红,盛热水的烧杯中酚酞试液变红,但放置后红色又消失了.盛热水的烧杯中酚酞试液变红、放置后红色又消失的原因是什么?
【作出猜想】甲同学认为可能是放入热水中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.小红则认为可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
【讨论交流】(1)小红认为甲同学的猜想不正确,请你阐述固体氢氧化镁不能使酚酞试液变色的原因:固体氢氧化镁中没有自由移动的OH-离子,不能使酚酞试液变红;乙同学认为上述酚酞试液变红、放置后红色又消失的现象还可能是由其他因素引起的.
【实验验证】(2)①乙同学设计了下列实验,请写出他的设计目的:
②小红设计了下列对比实验方案证明自己的猜想,请将其方案补充完整:
【提出问题】查阅元素周期表后发现钙元素和镁元素同在一个竖列里,她已经知道氢氧化钙溶液能使酚酞试液变红,她通过实验来探究不溶性的氢氧化镁是否也能使酚酞试液变红:将适量氢氧化镁分别加入到盛有冷水和热水的烧杯中,搅拌并分别向两烧杯中滴加酚酞试液,发现盛冷水的烧杯中酚酞试液没有变红,盛热水的烧杯中酚酞试液变红,但放置后红色又消失了.盛热水的烧杯中酚酞试液变红、放置后红色又消失的原因是什么?
【作出猜想】甲同学认为可能是放入热水中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.小红则认为可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
【讨论交流】(1)小红认为甲同学的猜想不正确,请你阐述固体氢氧化镁不能使酚酞试液变色的原因:固体氢氧化镁中没有自由移动的OH-离子,不能使酚酞试液变红;乙同学认为上述酚酞试液变红、放置后红色又消失的现象还可能是由其他因素引起的.
【实验验证】(2)①乙同学设计了下列实验,请写出他的设计目的:
| 实验步骤 | 设计目的 |
| 将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油 | 证明隔绝空气证明红色消失与氧气和二氧化碳无关. |
| 实验方法及可能观察到的现象 | 结论 | |
| 取A、B两支试管,都加入等质量的Mg(OH)2和等质量的热水,振荡,各滴入数滴无色酚酞. | 对A试管的操作及可观察到的现象温度保持不变;红色没褪去; | 红色消失与氢氧化镁的溶解度随温度降低而减小有关 |
| 对B试管的操作及可观察到的现象自然冷却;红色褪去. | ||
13.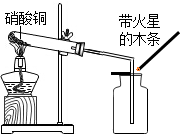 硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应
【查阅资料】
①氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O
②含氮化合物中,只有NO2是红棕色、有刺激性气味的气体.
③NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2.
【进行实验】
步骤II是同学们查阅了新的资料后设计完成的.该资料是关于NO2的沸点(或低温下NO2能否反应生成液态或固态物质)方面的性质信息.
【获得结论】
根据实验结果,Cu(NO3)2受热分解的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比.据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性.理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性.
 硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.【提出问题】硝酸铜在加热条件下到底发生了怎样的反应
【查阅资料】
①氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O
②含氮化合物中,只有NO2是红棕色、有刺激性气味的气体.
③NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2.
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤I:将反应后试管中的固体加水充分溶解,过滤,洗涤,向滤渣中加入足量稀硫酸,加热 | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜. |
步骤II:在如图的试管和集气瓶之间连上如图所示的装置,重新进行加热硝酸铜的实验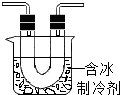 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解生成了氧气 |
【获得结论】
根据实验结果,Cu(NO3)2受热分解的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比.据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性.理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性.
14.人类每时每刻都离不开空气.空气成分按体积计,氧气约占( )
| A. | 78% | B. | 21% | C. | 50% | D. | 1% |
 如图所示,开始在气球中装有某种固体,在试管中装有某种液体,实验之前,气球是瘪的.实验时,把气球中的固体倒入试管中,发现气球慢慢变大.请你预测该固体和液体药品.(提示:可以填物质的化学式,也可以填物质的名称)
如图所示,开始在气球中装有某种固体,在试管中装有某种液体,实验之前,气球是瘪的.实验时,把气球中的固体倒入试管中,发现气球慢慢变大.请你预测该固体和液体药品.(提示:可以填物质的化学式,也可以填物质的名称)