题目内容
 如图是A、B、C三种物质的溶解度随温度变化的曲线图,根据图回答下列问题:
如图是A、B、C三种物质的溶解度随温度变化的曲线图,根据图回答下列问题:(1)图中M点表示的含义是
(2)随着温度的升高,A、B、C三种物质的饱和溶液中有溶质析出的是
(3)若A物质中含有少量的B物质,要提纯A时应采取的措施是
(4)T2℃时,3克A物质加入到10克水中,充分搅拌,得到A物质的
(5)现有T3℃时A、B、C三种物质的饱和溶液,若降温到T1℃时,三种物质的溶液中溶质的质量分数的关系是
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)溶解度曲线上的点表示该温度下物质的溶解度;
(2)析出晶体说明该物质的溶解度随温度的升高而减小;
(3)据AB的溶解度受温度变化情况分析提纯物质的方法;
(4)根据T2℃时A的溶解度是20g和溶解度的定义解答;
(5)根据ABC三种物质溶解度随温度的变化情况和溶质质量分数的计算公式分析判断.
(2)析出晶体说明该物质的溶解度随温度的升高而减小;
(3)据AB的溶解度受温度变化情况分析提纯物质的方法;
(4)根据T2℃时A的溶解度是20g和溶解度的定义解答;
(5)根据ABC三种物质溶解度随温度的变化情况和溶质质量分数的计算公式分析判断.
解答:解:(1)M点是AB溶解度曲线的交点,说明在该温度下二者的溶解度相等,故答案:T2℃使AB的溶解度都是20g;
(2)从溶解度曲线可以看出只有C的溶解度随温度的升高而减小,其余两种物质的溶解度都随温度的升高而增大,故答案:C;
(3)A的溶解度随温度升高而增大,B的溶解度受温度影响不大,所以当A物质中含有少量B物质时,用降温结晶提纯A,故答案:降温结晶;
(4)T2℃时A的溶解度是20g,说明该温度下100g水溶解20gA正好饱和,所以该温度下10g水中溶解2gA正好饱和,所以T2℃时,3克A物质加入到10克水中充分搅拌得到的是饱和溶液,只能溶解2gA,该溶液中溶质的质量分数为
×100%=16.7%;
(5)T3℃时A、B、C三种物质的饱和溶液,若降温到T1℃时AB都会析出晶体,C溶解度增大不会析出晶体溶质质量分数不变,所以C的溶质质量分数最小;T1℃时得到的还是AB的饱和溶液,此时B的溶解度最大,所以B溶液中溶质质量分数大于A中溶质质量分数,故答案选C.
(2)从溶解度曲线可以看出只有C的溶解度随温度的升高而减小,其余两种物质的溶解度都随温度的升高而增大,故答案:C;
(3)A的溶解度随温度升高而增大,B的溶解度受温度影响不大,所以当A物质中含有少量B物质时,用降温结晶提纯A,故答案:降温结晶;
(4)T2℃时A的溶解度是20g,说明该温度下100g水溶解20gA正好饱和,所以该温度下10g水中溶解2gA正好饱和,所以T2℃时,3克A物质加入到10克水中充分搅拌得到的是饱和溶液,只能溶解2gA,该溶液中溶质的质量分数为
| 2g |
| 2g+10g |
(5)T3℃时A、B、C三种物质的饱和溶液,若降温到T1℃时AB都会析出晶体,C溶解度增大不会析出晶体溶质质量分数不变,所以C的溶质质量分数最小;T1℃时得到的还是AB的饱和溶液,此时B的溶解度最大,所以B溶液中溶质质量分数大于A中溶质质量分数,故答案选C.
点评:本题考查了从溶解度曲线图读取信息、分析及获取信息的能力以及对溶解度概念的理解.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度的影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将下列四种家庭常用的调味品分别放入足量水中,不能形成溶液的是( )
| A、花生油 | B、味精 | C、食盐 | D、蔗糖 |
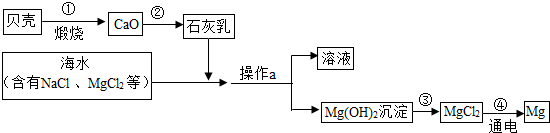
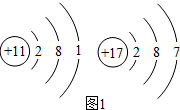 我们的日常生活离不开食盐,食盐的主要成分是氯化钠.
我们的日常生活离不开食盐,食盐的主要成分是氯化钠.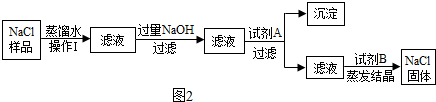
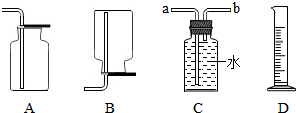 回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.
回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.