题目内容
12.2014年2月7日,索契冬季奥运会开幕式在回顾俄罗斯过去到未来的绚丽“梦境“中拉开了帷幕. 冬季奥运会需要大量材料.请回答:
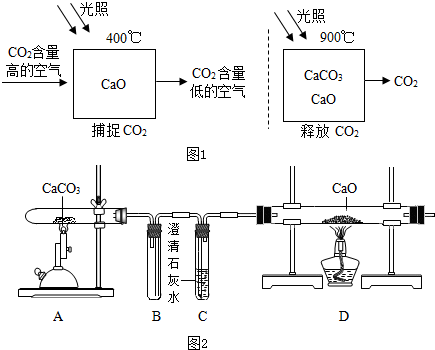
(1)图1应用中使用的材料属于金属材料是ABC(填序号);2014 年索契冬奥会的火炬,制造火炬的铝合金材料具有较好的抗腐蚀性,请解释:“铝的化学性质比较活泼,却具有较好的抗腐蚀性”:常温下铝表面能形成致密的氧化膜.
(2)冬奥会火种采集工作已于2013年9月29日在希腊奥林匹亚进行.火炬外形像神话传说中的火鸟.采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,点燃火炬.火炬传递结束后,采用关闭燃气阀门的方法熄灭火炬,其中蕴含的灭火原理是清除可燃物.采用丙烷(C3H8)作火炬燃料.丙烷燃烧时发出亮黄色火焰,反应生成水和二氧化碳,该反应的化学方程式为C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$4H2O+3CO2.
(3)冬奥运会对能量的需求很大.人类通过化学反应获得的能量,大多来自于天然气、石油和煤等化石燃料. 俄罗斯人在开发和使用新能源上进行了很多尝试,在街头发现一种不用外接电源的路灯(见图2,只要每天有短时间的光照就能使用,这种路灯使用的新能源是太阳能.
分析 (1)根据金属材料的分类来分析;根据铝的性质来分析;
(2)根据化学方程式的书写方法,灭火方法考虑;
(3)化石燃料包括煤、石油、天然气;根据提供的信息判断.
解答 解:(1)ABC均属于利用金属材料制成的,在常温下,铝易与空气中的氧气反应生成致密结实的氧化铝薄膜,对内部结构起到了保护作用;
(2)关闭燃气阀门的方法熄灭火炬,是将可燃物隔离了,没有了可燃物就不能燃烧了;C3H8在空气中完全燃烧的反应物是C3H8和氧气,生成物是二氧化碳和水,先配平碳和氢,最后配平氧,反应条件是点燃,写在等号的上边;所以方程式是:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O;
(3)化石燃料包括煤、石油、天然气;根据信息:只要每天有短时间的光照就能使用.可知这种路灯使用的新能源是太阳能.
故答案为:
(1)ABC;常温下铝表面能形成致密的氧化膜
(2)清除可燃物; C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$4H2O+3CO2
(3)石油;太阳能.
点评 本题即考查金属材料、金属的性质以及化石燃料的种类,又考查化学反应式的书写和燃烧的条件,是综合类题目,但难度不大,属于基础知识.

练习册系列答案
相关题目
3.有一种神奇的蜡烛,点燃任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究.
查阅资料:普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛燃烧时,金属并不燃烧但当蜡烛吹灭后,未冷却的金属接触到氧就发生燃烧,从而使蜡烛复燃.
老师告诉同学们,蜡烛芯内打火石中的某种金属可能是镁、铁或铜中的一种,为确定该金属的成分,大家设计了以下实验方案,请你填空和回答有关问题(注:不考虑打火石中稀土元素对探究金属性质的影响).
反思交流:
(1)实验2中反应的化学方程式为Mg+2HCl═MgCl2+H2↑.
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以燃烧.
(3)这种“吹不灭”的蜡烛实际上也可以熄灭,你采用的方法是隔绝氧气或剪除灯芯或用湿抹布盖灭等.
查阅资料:普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛燃烧时,金属并不燃烧但当蜡烛吹灭后,未冷却的金属接触到氧就发生燃烧,从而使蜡烛复燃.
老师告诉同学们,蜡烛芯内打火石中的某种金属可能是镁、铁或铜中的一种,为确定该金属的成分,大家设计了以下实验方案,请你填空和回答有关问题(注:不考虑打火石中稀土元素对探究金属性质的影响).
| 实验 | 操作步骤 | 实验现象 | 实验结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石呈银白色 | 该金属一定不是铜 |
| 2 | 取少量打磨后的打火石与试管中,滴加稀盐酸. | 有无色气体产生 | 该金属一定不是铁,而是镁 |
(1)实验2中反应的化学方程式为Mg+2HCl═MgCl2+H2↑.
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以燃烧.
(3)这种“吹不灭”的蜡烛实际上也可以熄灭,你采用的方法是隔绝氧气或剪除灯芯或用湿抹布盖灭等.
20.下列图示实验操作中,正确的是( )
| A. |  测定溶液的pH | B. |  稀释浓硫酸 | C. |  蒸发食盐水 | D. |  点燃酒精灯 |
1.据媒体所道,今年中纪委宣布反腐的重区是“中管金融”和“华能”“国电”“船舶”等国企.钛合金具有强抗腐蚀性能,是舰船生产必不可少的材料.下列物质不属于合金的是( )
| A. | 黄铜 | B. | 青铜 | C. | 生铁 | D. | 四氧化三铁 |
11.氧是地壳中含量最多的元素,有两种氧原子可以分别表示为为${\;}_{8}^{16}$O和${\;}_{8}^{18}$O右下角数字表示质子数,右上角数字为质子数和中子数之和,则( )
| A. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O互为同位素 | |
| B. | ${\;}_{8}^{16}$O的核外电子数多于${\;}_{8}^{18}$O | |
| C. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O属于同种原子 | |
| D. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O的核内中子数相等 |