题目内容
17. A、B、C、D、E是初中化学课本中常涉及到的五种不同类别的物质,A为单质,C在农业上常用来改良酸性土壤,D在工业上可以除铁锈,请你仔细阅读和思考后回答下列有关问题:
A、B、C、D、E是初中化学课本中常涉及到的五种不同类别的物质,A为单质,C在农业上常用来改良酸性土壤,D在工业上可以除铁锈,请你仔细阅读和思考后回答下列有关问题:(1)A、D的化学式分别为H2、HCl.
(2)B→C的化学方程式为H2O+CaO=Ca(OH)2.
(3)C与E反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(4)物质E应具备的条件是复分解反应的条件.
分析 根据“C在农业上常用来改良酸性土壤”,则推测C为氢氧化钙;根据“D在工业上可以除铁锈”,则推测D为稀盐酸;根据“A为单质”,则推测A可能为氢气;结合图框:推测B可能为水,E为碳酸钠,代入检验.
解答 解:
根据“C在农业上常用来改良酸性土壤”,则推测C为氢氧化钙;根据“D在工业上可以除铁锈”,则推测D为稀盐酸;根据“A为单质”,则推测A可能为氢气;结合图框:推测B可能为水,E为碳酸钠,代入检验.
(1)根据分析,A、D的化学式分别为H2、HCl.
(2)根据分析,B可能为水,C为氢氧化钙,则B→C的化学方程式为H2O+CaO=Ca(OH)2.
(3)根据分析,C为氢氧化钙,E为碳酸钠,故C与E反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(4)物质E应具备的条件是复分解反应的条件.
故答案为:
(1)H2、HCl.(2)H2O+CaO=Ca(OH)2.
(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.(4)复分解反应的条件.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
7.将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混合溶液中,充分反应后过滤,得到滤液M和滤渣N.下列有关说法中,合理的是( )
| A. | 滤液M中可能存在Fe2+ | |
| B. | 滤液M中一定含有两种金属阳离子 | |
| C. | 滤渣N中一定没有单质镁 | |
| D. | 滤渣N的质量一定大于加入铁粉的质量 |
8.下列元素属于人体所需微量元素的是( )
| A. | 锌 | B. | 氧 | C. | 钙 | D. | 氢 |
5.下列方法不能达到实验目的是( )
| A. | 用水区分烧碱和硝酸铵两种固体 | |
| B. | 用硝酸银溶液区分氯化钠和氯化钙溶液 | |
| C. | 除去氧化铜中含有的铜粉:在空气中加热 | |
| D. | 除去二氧化碳中含有的水蒸气,将气体通过浓硫酸 |
9.检查玻璃器具洗净的标准是内壁( )
| A. | 不挂水珠 | B. | 透明 | C. | 无异味 | D. | 光滑 |
6.下列化学用语表达正确的是( )
| A. | 氯酸钾中氯元素的化合价:K$\stackrel{+3}{Cl}$O3 | |
| B. | 镁离子的结构示意图: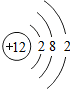 | |
| C. | 两个乙醇分子:2C2H5OH | |
| D. | 工业上炼铁的主要反应原理:3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ |