题目内容
14.用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:第一步:将集气瓶容积划分为五等份,并做好标记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.

第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的$\frac{1}{5}$.
请回答下列问题:
(1)红磷在集气瓶内燃烧的现象剧烈地燃烧,放出大量的热,产生大量白烟,反应的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$ 2P2 O5.
(2)实验完毕,若进入集气瓶中水的体积不到总容积的$\frac{1}{5}$,你认为导致这一结果的原因可能是装置漏气.
(3)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是装置始终密闭,空气没有逸出,实验结果准确.
分析 (1)根据红磷在点燃条件下能和空气中的氧气反应生成五氧化二磷;结合化学方程式的书写进行分析;
(2)根据实验完毕,若进入集气瓶中水的体积不到总容积的五分之一,说明瓶内气体减少量不足五分之一,分析其原因主要为氧气未完全消耗或是冷却过程中空气进入瓶中所导致的结果,据此对实验进行分析;
(3)对比改进行前后的两种探究装置,可发现改进后不需要点燃红磷后再将燃烧匙伸入瓶中,可很好地避免因装置漏气而对结果带来的偏差.
解答 解:
(1)红磷燃烧的现象是:剧烈地燃烧,放出大量的热,产生大量白烟;红磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$ 2P2 O5;
(2)如果实验中因红磷量不足而氧气没有完全消耗或因装置漏气而在冷却过程中进入少量空气或未冷却至室温而打开弹簧夹等,都可能出现进入集气瓶中水的体积不到总容积的五分之一的结果;
(3)改进后的装置直接通过聚太阳光而引燃磷,避免了再次打开瓶塞而保持装置始终密封,减少了操作中人为因素所造成的偏差,可得到更准确的实验结果.
故答案为:
(1)剧烈地燃烧,放出大量的热,产生大量白烟过量;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$ 2P2 O5;
(2)装置漏气;
(3)装置始终密闭,空气没有逸出,实验结果准确.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.为了增强植物抗倒伏的能力,应该施用钾肥.下列化肥属于钾肥的是( )
| A. | 碳酸氢铵 | B. | 氯化钾 | C. | 硫酸铵 | D. | 磷矿粉 |
2.通过学习碱的性质,某校化学兴趣小组的同学对实验室的“氢氧化钙是否变质以及变质的程度”展开了探究活动,请你一同参与.
(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:同学们经过讨论认为样品存在三种可能情况:没有变质;部分变质;完全变质.
如果氢氧化钙变质,变质的化学方程多为:Ca(OH)2+CO2═CaCO3↓+H2O.
(3)实验探究:补充填空.
(4)小结与思考:
①小蔓同学根据上述实验方案进行实验,确定该样品已部分变质,请写出实验中反应涉及的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑
②氢氧化钙俗称熟石灰,农业上常用来改良酸性土壤等.
(5)某工厂化验室用氢氧化钠溶液中和一定量石油产品中的残余硫酸至中性,共消耗5%的氢氧化钠溶液80g.这一定量石油产品中含H2SO4的质量是多少?
(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:同学们经过讨论认为样品存在三种可能情况:没有变质;部分变质;完全变质.
如果氢氧化钙变质,变质的化学方程多为:Ca(OH)2+CO2═CaCO3↓+H2O.
(3)实验探究:补充填空.
| 实验步骤及操作 | 实验现象 | 实验结论 |
| ①取样于试管中,加入足量蒸馏水振荡,静置取上层清液,滴入无色酚酞溶液; ②倒去上层清液,再向试管中注入稀盐酸 | ①无色酚酞溶液变红; ②有气泡产生 | 部分变质 |
| ①无色酚酞溶液不变红; ②有气泡产生 | 全部变质 | |
| ①无色酚酞试液变红; ②没有气泡产生 | 没有变质 |
①小蔓同学根据上述实验方案进行实验,确定该样品已部分变质,请写出实验中反应涉及的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑
②氢氧化钙俗称熟石灰,农业上常用来改良酸性土壤等.
(5)某工厂化验室用氢氧化钠溶液中和一定量石油产品中的残余硫酸至中性,共消耗5%的氢氧化钠溶液80g.这一定量石油产品中含H2SO4的质量是多少?
6.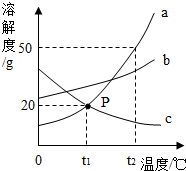 如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
 如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )| A. | t1℃时三种物质溶解度的大小为b>a=c | |
| B. | 将t2℃时a的饱和溶液150g降温到t1℃时,析出溶质30g | |
| C. | 除去a物质中的少量c,通常采用蒸发结晶的方法 | |
| D. | t2℃时1g a物质加入到2g水中不断搅拌,能形成3g饱和溶液 |
3.某小组同学用盐酸和氢氧化钙,对酸和碱的中和反应进行探究.请你参与.
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
【提出问题】甲实验后的溶液中有什么溶质?
【作出猜想】猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
【实验探究】为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
【实验结论】丙认为猜想三正确.
【实验评价】丙的实验操作和方案中有不足之处,其不足之处是方案1中使用pH试纸的操作不对;方案2中加AgNO3产生白色沉淀说明溶液中有Cl-,并不能说明溶液中一定有CaCl2.
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.实验中观察到的现象涉及的反应化学方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl(任意写一个).
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
【提出问题】甲实验后的溶液中有什么溶质?
【作出猜想】猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
【实验探究】为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量甲实验后的溶液于试管中) | 镊子pH试纸 | AgNO3溶液 | Na2CO3溶液 |
| 实验现象 | 对比标准比色卡:pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有CaCl2 |
【实验评价】丙的实验操作和方案中有不足之处,其不足之处是方案1中使用pH试纸的操作不对;方案2中加AgNO3产生白色沉淀说明溶液中有Cl-,并不能说明溶液中一定有CaCl2.
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.实验中观察到的现象涉及的反应化学方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl(任意写一个).
4.下列实验操作中,错误的是( )
| A. |  加热液体 | B. | 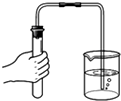 检查装置气密性 | C. | 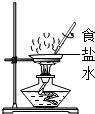 蒸发食盐水 | D. | 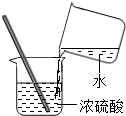 稀释浓硫酸 |