题目内容
19.请根据初中常见的物质和反应,回答以下问题:(1)常在实验室中用作干燥剂的液体是(写名称)浓硫酸.
(2)化石燃料燃烧会导致酸雨的主要气体污染物是(写化学式)SO2.
(3)将生锈的铁钉放入过量的稀盐酸中,可观察到的现象为铁锈溶解、生成黄色溶液,然后观察到有气泡冒出.
分析 (1)根据干燥剂的种类和状态进行分析;
(2)化石燃料燃烧会导致酸雨的主要气体污染物是二氧化硫;
(3)把生锈的铁钉放到足量的稀盐酸中,表面的铁锈先与盐酸反应,当铁锈反应完后,铁继续与盐酸反应,据此分析现象.
解答 解:(1)常见的干燥剂有氢氧化钠固体和浓硫酸,又是液体,所以是浓硫酸,故答案为:浓硫酸;
(2)化石燃料燃烧会导致酸雨的主要气体污染物是二氧化硫,故答案为:SO2;
(3)锈的主要成分是Fe2O3,它会与稀盐酸反应,生成的Fe3+显黄色,其反应的化学方程式为:Fe2O3 +6HCl═2FeCl3+3H2O,当铁锈反应完后,铁继续与盐酸反应,该反应的化学方程式为:Fe+2HCl═FeCl2+H2↑,所以会观察到有气泡冒出;故答案为:铁锈溶解、生成黄色溶液,然后观察到有气泡冒出.
点评 本题难度不大,掌握浓硫酸与常见物质的性质,实验现象的描述是正确解答本题的关键.

练习册系列答案
相关题目
7.如图所示的化学实验基本操作中,正确的是( )
| A. | 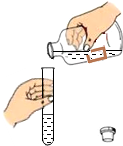 倾倒液体 | B. | 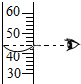 读取数值 | C. | 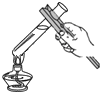 加热液体 | D. | 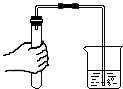 检查气密性 |
4. 用如图所示的装置进行电解水实验,有以下描述:
用如图所示的装置进行电解水实验,有以下描述:
①该实验可以证明水是由氢元素与氧元素组成的
②甲、乙两试管内收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧
④甲、乙两试管内收集到的气体的质量比约为1:8
以上描述中正确的是( )
 用如图所示的装置进行电解水实验,有以下描述:
用如图所示的装置进行电解水实验,有以下描述:①该实验可以证明水是由氢元素与氧元素组成的
②甲、乙两试管内收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧
④甲、乙两试管内收集到的气体的质量比约为1:8
以上描述中正确的是( )
| A. | ①②③④ | B. | ①③ | C. | ①② | D. | ①②③ |
11.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】①溶质可能只是CaCl2
②溶质可能是CaCl2与Ca(OH)2
③溶质可能是CaCl2与HCl
【实验探究】小明同学为了探究溶液中溶质的成分,进行了以下实验探究:
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁制下水道,可能造成的危害是腐蚀铁制下水道.要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量碳酸钙,充分反应后过滤.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】①溶质可能只是CaCl2
②溶质可能是CaCl2与Ca(OH)2
③溶质可能是CaCl2与HCl
【实验探究】小明同学为了探究溶液中溶质的成分,进行了以下实验探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,向试管中滴加几滴无色酚酞溶液,振荡 | 溶液不变色 | 猜想②不正确 |
| 猜想③正确 |
8.ClO2是新一代自来水消毒剂.如图为制取ClO2反应的微观示意图.下列有关该反应的说法正确的是( )
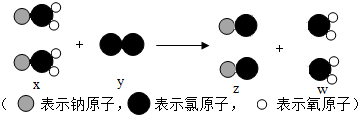

| A. | 该反应的化学方程式为:2NaClO2+Cl2═2NaCl+ClO2 | |
| B. | x是化合物,y单质 | |
| C. | z、w都是氧化物 | |
| D. | 该反应属于置换反应 |
