题目内容
5.推理是化学学习中常用的思维方法.下列推理正确的是( )| A. | 利用红磷燃烧可测定空气中氧气的含量,木炭能燃烧,也可测定空气中氧气的含量 | |
| B. | 溶液一定是均一、稳定的,则均一、稳定的物质一定是溶液 | |
| C. | 盐是由金属离子和酸根离子组成的,NH4NO3中没有金属元素,所以不属于盐 | |
| D. | NaOH溶液中的OH-能与酸反应,则KOH溶液中的OH-也能与酸反应 |
分析 A、根据木炭燃烧生成二氧化碳气体进行考虑;
B、根据溶液的概念进行考虑;
C、根据铵盐考虑本题;
D、根据碱的性质考虑.
解答 解:A、木炭燃烧生成二氧化碳气体,不能用来测定空气中氧气的含量,故错;
B、均一、稳定的物质不一定是溶液,例如水,故错;
C、NH4NO3中没有金属元素,但属于铵盐,故错;
D、氢氧化钠、氢氧化钾都属于碱,碱能与酸发生中和反应,反应的实质就是氢氧根离子与氢离子反应生成水,故正确.
故选:D.
点评 解答本题关键是要知溶液的定义、盐的概念以及酸碱中和反应,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.在学习碱的化学性质时,某小组同学进行了如下图实验,
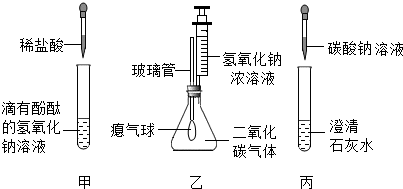
Ⅰ.探究碱的化学性质
①实验甲,随着稀盐酸的不断滴入,观察到溶液由红色变为无色;
②实验乙,滴加氢氧化钠溶液后,观察到气球变鼓
③实验丙,观察到试管内有白色沉淀产生,发生反应得化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Ⅱ.探究非也成分
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【查阅资料】BaCl2溶液呈中性且Na2CO3+BaCl2═BaCO3↓+2NaCl
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和氯化钠;
②还含有能使废液呈碱性的物质,同学们有如下猜想:
猜想1:碳酸钠;猜想2:氢氧化钠;
猜想3:氢氧化钠和碳酸钠;猜想4:氢氧化钠和氢氧化钙;
【实验设计】
同学们认为需要先验证猜想4是否成立,所需要的试剂是碳酸钠溶液,
若猜想4不成立,则需要进行后续实验,请你完成表格.
【进行实验】同学们进行实验,通过实验现象,得出了猜想2成立.

Ⅰ.探究碱的化学性质
①实验甲,随着稀盐酸的不断滴入,观察到溶液由红色变为无色;
②实验乙,滴加氢氧化钠溶液后,观察到气球变鼓
③实验丙,观察到试管内有白色沉淀产生,发生反应得化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Ⅱ.探究非也成分
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【查阅资料】BaCl2溶液呈中性且Na2CO3+BaCl2═BaCO3↓+2NaCl
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和氯化钠;
②还含有能使废液呈碱性的物质,同学们有如下猜想:
猜想1:碳酸钠;猜想2:氢氧化钠;
猜想3:氢氧化钠和碳酸钠;猜想4:氢氧化钠和氢氧化钙;
【实验设计】
同学们认为需要先验证猜想4是否成立,所需要的试剂是碳酸钠溶液,
若猜想4不成立,则需要进行后续实验,请你完成表格.
| 实验操作 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钡溶液,静置 | 有白色沉淀,溶液无色 | 猜想1正确 |
| 若没有白色沉淀,溶液呈红色 | 猜想2正确 | |
| 有白色沉淀,溶液呈红色 | 猜想3正确 |
20.物质的用途和性质密切相关.下列用途主要是利用其物理性质的是( )
| A. |  石墨制铅笔芯 | B. |  氧气用于金属切割 | ||
| C. |  食品充氮防腐 | D. |  熟石灰改良酸性土壤 |
14.下列说法中,正确的是( )
| A. | 家用电器着火,立即用水泼灭 | |
| B. | 日常生活中,用生石灰做干燥剂 | |
| C. | 发令枪中红磷燃烧时产生大量“白雾” | |
| D. | 生铁和钢都是铁合金,在用途上没有区别 |
18.下列有关推理中,正确的是( )
| A. | 复分解反应生成两种化合物,则生成两种化合物的反应一定是复分解反应 | |
| B. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| C. | 有机物都含碳元素,所以含碳元素的化合物一定是有机物 | |
| D. | 酸性溶液能使石蕊溶液变红,则使石蕊溶液变红的一定是酸性溶液 |
