题目内容
13.(1)高铁酸钠(Na2Fe04)是一种新型高效的净水剂,高铁酸讷中铁元素的化合价为+6;(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.请将下列脱氧剂中的主要反应的化学方程式补充完整:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 (1)根据在化合物中正负化合价代数和为零,结合高铁酸钠(Na2FeO4)的化学式进行解答本题;
(2)根据化学反应前后原子的种类和数目不变进行解答.
解答 解:(1)钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.故填:+6;
(2)化学反应前后各元素的原子个数不变,反应后含有4个Fe原子,12个O原子,12个H原子,反应前含有4个Fe原子,10个O原子,8个H原子,故该物质的一个分子中含有2个H原子和一个O原子,其化学式为H2O.故填:H2O.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法以及质量守恒定律即可正确解答本题.

练习册系列答案
相关题目
11.将少量下列物质分别放到水中,充分搅拌,不能得到溶液的是( )
| A. | 硝酸钾 | B. | 氯化钠 | C. | 高锰酸钾 | D. | 碳酸钙 |
4. 实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
【提出问题1】该样品中含有那些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:全部是NaOH 猜想Ⅱ:已完全变质,该样品中只含Na2CO3;
猜想Ⅲ:部分变质,该样品中含有NaOH和Na2CO3.
【查阅资料】CO2在饱和碳酸氢钠溶液中几乎不溶解.
【实验探究1】为确定该样品的成分,小明设计了如表实验方案,请你一起完成下列实验报告.
回答下列问题(1)实验室中,氢氧化钠固体应怎样保存?密封保存
(2)用酚酞试液不能(填“能”或“不能”)检验氢氧化钠变质.
(3)若取少量的固体溶于水,滴加几滴稀盐酸,没有气泡产生.不能(填“能”或“不能”)证明氢氧化钠固体没有变质.
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】小红同学设计如图所示装置(铁架台略去),实验在20℃,101kPa下进行,步骤如下:
①按图连接好装置;
②检查装置气密性
③用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
④向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢钠溶液224mL.
请回答下列问题:
(1)B中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由避免CO2溶解在水中有损耗,导致测定结果偏低.
(2)试管中原有的空气对实验结果没有明显影响理由是因为试管中原有空气的体积与反应后试管中没有排尽的二氧化碳的体积几乎等同.
(3)变质氢氧化钠样品中碳酸钠的质量分数为53%(20℃,101kPa下,22.4L二氧化碳的质量为44g)
【拓展提高】已知Na2CO3溶液与稀硫酸反应先生成NaHCO3,当Na2CO3全部转化为NaHCO3后,生成的NaHCO3能继续与稀硫酸反应生成CO2.现向样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液.请分析推断反应后所得X溶液的溶质,其所有的可能组成Na2SO4和NaHCO3、Na2SO4、Na2SO4H2SO4.
 实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.【提出问题1】该样品中含有那些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:全部是NaOH 猜想Ⅱ:已完全变质,该样品中只含Na2CO3;
猜想Ⅲ:部分变质,该样品中含有NaOH和Na2CO3.
【查阅资料】CO2在饱和碳酸氢钠溶液中几乎不溶解.
【实验探究1】为确定该样品的成分,小明设计了如表实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 1)取少量样品溶于水,加入过量的CaCl2溶液 | 白色沉淀产生 | 该反应的化学方程式:CaCl2+Na2CO3=2NaCl+CaCO3 氢氧化钠已经变质 |
| 2)将上述反应后的混合物过滤,取滤液加入酚酞溶液 | 变红 | 证明猜想Ⅲ正确 |
(2)用酚酞试液不能(填“能”或“不能”)检验氢氧化钠变质.
(3)若取少量的固体溶于水,滴加几滴稀盐酸,没有气泡产生.不能(填“能”或“不能”)证明氢氧化钠固体没有变质.
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】小红同学设计如图所示装置(铁架台略去),实验在20℃,101kPa下进行,步骤如下:
①按图连接好装置;
②检查装置气密性
③用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
④向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢钠溶液224mL.
请回答下列问题:
(1)B中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由避免CO2溶解在水中有损耗,导致测定结果偏低.
(2)试管中原有的空气对实验结果没有明显影响理由是因为试管中原有空气的体积与反应后试管中没有排尽的二氧化碳的体积几乎等同.
(3)变质氢氧化钠样品中碳酸钠的质量分数为53%(20℃,101kPa下,22.4L二氧化碳的质量为44g)
【拓展提高】已知Na2CO3溶液与稀硫酸反应先生成NaHCO3,当Na2CO3全部转化为NaHCO3后,生成的NaHCO3能继续与稀硫酸反应生成CO2.现向样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液.请分析推断反应后所得X溶液的溶质,其所有的可能组成Na2SO4和NaHCO3、Na2SO4、Na2SO4H2SO4.
1.在元素周期表中,应用于计算机芯片的硅元素如图所示,下列硅的说法正确的是( )


| A. | 原子序数是14 | B. | “--”中硅元素符号是SI | ||
| C. | 相对原子质量是14 | D. | 质子数是28.05 |
18.下列说法正确的是( )
| A. | 混合物一定由不同种分子构成 | B. | 化合物中一定含有不同种元素 | ||
| C. | 只含有一种元素的物质一定是单质 | D. | 含有氧元素的物质一定是氧化物 |
2.某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多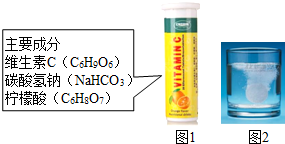 气泡产生(如图2).该小组同学进行如下探究.
气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、
N2.
小明说:不可能含有N2,因为维C泡腾片和水中无氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,
H2易燃易爆,CO 有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有CO2.写出该反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 气泡产生(如图2).该小组同学进行如下探究.
气泡产生(如图2).该小组同学进行如下探究.探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、
N2.
小明说:不可能含有N2,因为维C泡腾片和水中无氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,
H2易燃易爆,CO 有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有CO2.写出该反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.