题目内容
3.稀释浓硫酸时,一定要把浓硫酸沿着容器壁慢慢地注入水中.表面生锈的铁钉放入适量稀硫酸中,无色液体逐渐变成黄色反应的方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.分析 根据浓硫酸的稀释方法、铁锈的主要成分是氧化铁,能与稀硫酸反应生成硫酸铁和水,据此进行分析解答.
解答 解:稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中.
表面生锈的铁钉放入适量稀硫酸中,铁锈的主要成分是氧化铁,与稀硫酸反应生成硫酸铁和水,会观察到无色液体逐渐变成黄色,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故答案为:浓硫酸;水;黄色;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
点评 本题难度不大,掌握浓硫酸的稀释方法、酸的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
16.要除去下列物质中混有的少量杂质(括号内为杂质),所用的试剂和操作都正确的是( )
| A. | CaCl2固体(CaCO3);加足量稀硫酸、蒸发、结晶 | |
| B. | NaCl固体(Na2CO3);加足量稀盐酸、蒸发、结晶 | |
| C. | Fe粉(Cu);加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | N2(CO);通过灼热的氧化铜 |
18.章章和卢卢都非常喜欢做科学探究实验,不仅能动脑筋思考,同时还锻炼了自己的动手能力提高了处理特殊情况的能力.下列有关他俩儿对实验设计的方案中,达不到实验目的是( )
| A. | 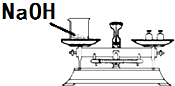 称取氢氧化钠固体 | |
| B. | 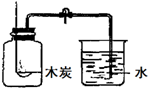 探究空气中氧气体积分数 | |
| C. | 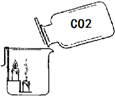 验证CO2 密度比空气大且不能燃烧也不支持燃烧 | |
| D. | 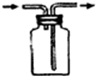 收集H2 |


