题目内容
3.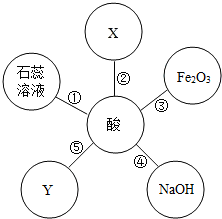 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.(1)图中①的现象是:石蕊溶液变红色.
(2)已知X是金属单质,则X可以是:锌(填一种即可).
(3)若此酸为稀硫酸,反应③的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(4)若此酸为稀盐酸,测得反应 ④得到的溶液pH>7,则溶质为NaOH、NaCl.
(5)若稀盐酸与属于Y的2种物质均反应,不仅有使澄清石灰水变浑浊的气体产生且产物完全相同,则反应⑤的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑、Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 根据已有的酸的性质进行分析解答即可,酸能与指示剂、活泼金属、金属氧化物、碱以及盐发生反应,据此解答.
解答 解:(1)酸能使石蕊试液变化红,故填:石蕊溶液变红;
(2)氢前的金属能与酸反应,故可以是金属锌,故填:锌;
(3)稀硫酸能与氧化铁反应生成硫酸铁和水,故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)氢氧化钠和盐酸反应生成氯化钠和水,溶液的pH大于7,说明呈碱性,含有氢氧化钠,故填:NaOH、NaCl;
(5)Y是盐,碳酸钠呢碳酸氢钠都能与盐酸反应生成氯化钠、水和二氧化碳,故填:NaHCO3+HCl=NaCl+H2O+CO2↑,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题考查的是常见的酸的性质,完成此题,可以依据已有的酸的通性进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.除去下列物质中含有的杂质,选用的方法正确的是( )
| 物质 | 所含杂质 | 方法 | |
| A | N2 | O2 | 通过灼热的铜丝 |
| B | CaO | CaCO3 | 加入适量的稀盐酸 |
| C | CO2 | HCl | 通过足量的氢氧化钠溶液 |
| D | NaCl溶液 | Na2CO3 | 加入适量的Ca(NO3)2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
14.下列化学用语书写正确的是( )
| A. | 2个氢原子-H2 | B. | 3个铁离子-3Fe2+ | ||
| C. | 氧化铝-Al2O3 | D. | +2价的镁元素-Mg2+ |
18.下列应用与中和反应原理无关的是( )
| A. | 用熟石灰改良酸性土壤 | |
| B. | 用浓硫酸干燥湿润的氧气 | |
| C. | 用肥皂水涂在被蚊虫叮咬的皮肤上止痒 | |
| D. | 用氢氧化钠溶液洗涤石油产品中的残留硫酸 |
15.火箭燃料(习惯上称燃烧剂和氧化剂的混合物为燃料,又称推进剂)是制约航空航天事业发展的一个重要因素,燃料的燃烧效率是用比冲量来度量的,即燃烧1kg燃料能持续多少秒一直产生1kg的推力.以比冲量为衡量标准,下列四种常见火箭燃料中,最理想的组合是( )
| 选项 | 燃烧剂 | 氧化剂 | 比冲量/s |
| A | 煤油 | 液态氧 | 240 |
| B | 乙醇 | 液态氧 | 254 |
| C | 偏二甲肼 | 四氧化二氮 | 225~258 |
| D | 液态氢 | 液态氧 | 35~425 |
| A. | A | B. | B | C. | C | D. | D |
16.化学与生活密切相关,下列说法正确的是( )
| A. | 在煤炉上放一盆水可防止煤气中毒 | |
| B. | 用铅笔芯的粉末可使锁的开启变得灵活 | |
| C. | 胃酸过多的病人在空腹时最好多喝一些柠檬汁 | |
| D. | 有人不慎跌入多年未开启的菜窖时,不必采取防护措施,立即下洞救人 |