题目内容
18. 以下装置可用于实验室制取气体,请回答下列问题.
以下装置可用于实验室制取气体,请回答下列问题.( 1)实验室制取氧气可选择的发生装置A( 填序号 ),该装置中发生反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若用装置 C 收集 O2,验满的方法是将带火星的木条放在a导管出口,木条复燃证明氧气已集满.
(2)实验室制取 CO2所用的药品是大理石(或石灰石)和稀盐酸.若要收集干燥的 CO2,需将气体通过 C 装置后再收集,C 装置中盛装的试剂是浓硫酸,进气口是b(填“a”或“b”).试验结束后,B 装置中剩余药品 的处理方法是液体倒入废液缸,固体洗净后放入指定容器.
分析 (1)根据实验室制取氧气的药品状态和反应条件选择发生条件和书写化学方程式,氧气有助燃性,可用带火星的木条检验;
(2)实验室用大理石(或石灰石)和稀盐酸反应制取二氧化碳,浓硫酸有吸水性可用来干燥气体,洗气瓶在使用时要长进短出,实验结束后废液要倒入废液桶.
解答 解:(1)制取氧气可以用高锰酸钾加热的方法,此时要选择A装置做为发生装置,也可以用过氧化氢和二氧化锰来制取氧气,此时要选择不用加热的B装置,用高锰酸钾加热制氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用过氧化氢制氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;氧气有助燃性,可以用带火星的木条来检验,检验时将带火星的木条放在a导管出口,木条复燃证明氧气已集满.
(2)实验室用大理石(或石灰石)和稀盐酸反应来制取二氧化碳,二氧化碳可用具有吸水性的浓硫酸来干燥,使用洗气瓶时要长管通入,短管通出,故进气口为b,剩余药品的处理方法分为液体和固体,答案应为:液体倒入废液缸,固体洗净后放入指定容器.
故答案为:(1)A(或B);2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑); 将带火星的木条放在a导管口,木条复燃证明氧气已集满;
(2)大理石(或石灰石)和稀盐酸;浓硫酸;b;液体倒入废液缸,固体洗净后放入指定容器.
点评 本题考查了气体的制取,气体的制取是初中重要的化学实验之一,既是难重点,又是考查热点,理解反应原理,掌握装置的选择依据、气体的检验、验满、收集方法,了解实验步骤和注意事项是解决该类问题的关键.

| A. | 炒菜用的铁锅应在干燥的地方存放 | |
| B. | 黄铜的硬度比铜的硬度大,其抗腐蚀性也比铜好很多 | |
| C. | 生活中常把铝块制成铝箔,这是利用了铝的延展性 | |
| D. | 铝的金属活动顺序位于氢的前面,因而铝在自然界中以单质的形式存在 |
| 物质 | 选用试剂 | 主要操作 | |
| A | CO2(CO) | CuO | 通过足量的灼热氧化铜 |
| B | MnO2(KCl) | H2O | 过滤 |
| C | NaCl(CuCl2) | AgNO3溶液 | 结晶 |
| D | Fe(Zn) | H2SO4溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
| N2 | CO2 | O2 | H2O | |
| 物质的量分数 | 0.7110 | 0.0810 | 0.0225 | 0.1710 |
(1)燃料混合气中甲烷与氢气的物质的量之比
(2)燃料混合气与空气的物质的量之比.
| A. | Al | B. | Cl | C. | Ag | D. | Si |
| A. | 打开浓盐酸瓶口产生白烟,说明浓盐酸有挥发性 | |
| B. | 稀盐酸中滴入紫色石蕊试液,溶液变红,说明酸遇指示剂变色 | |
| C. | 滴有品红的水呈红色,通过活性炭后变无色,说明活性炭具有吸附性 | |
| D. | 硫在空气中燃烧发出蓝紫色火焰,说明硫具有可燃性 |
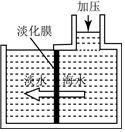 海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )
海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )| A. | 淡化膜可以换成滤纸 | B. | 右侧溶剂质量减少 | ||
| C. | 左侧溶液质量不变 | D. | 右侧溶质质量分数减少 |
| A. | 室内起火时,应立即打开所有门窗进行呼救 | |
| B. | 用工业用盐(亚硝酸钠)烹调食物 | |
| C. | 用甲醛溶液浸泡食用海产品以保鲜 | |
| D. | 烧菜时油锅着火,立即盖上锅盖 |