题目内容
10.现有Fe、稀H2SO4、Na2CO3溶液、Ca(OH)2溶液、Fe2O3两两混合后,能发生反应的有( )| A. | 7个 | B. | 6个 | C. | 5个 | D. | 4个 |
分析 利用所学的化学反应知识结合复分解反应的发生条件,对所列物质进行两两组合找到可反应的组合
解答 解:利用各种反应的发生要求可知Fe、稀H2SO4、Na2CO3溶液、Ca(OH)2溶液、Fe2O3两两混合后,Fe和稀H2SO4能反应,稀H2SO4和Na2CO3溶液能反应,稀H2SO4和Ca(OH)2溶液能反应,稀H2SO4和Fe2O3能反应,Na2CO3溶液和Ca(OH)2溶液能反应,一共5个反应.
故选C.
点评 此题是对物质间反应的考查,解题的重点是对反应的发生条件要有明确的认识,属基础性知识考查题.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
20. 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热.同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热.待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热.同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热.待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使空气中的氧气充分反应.
(2)写出该实验中反应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(3)小强测得实验结果如下:
由此数据可以推算出他测定的空气中氧气的体积分数<21%(填“>”、“=”或“<”).造成该实验出现误差的原因可能是①②③.(填序号)
①没有交替缓缓推动两个注射器活塞 ②读数时没有冷却至室温 ③加入铜丝量太少 ④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.(其它答案合理也可).
 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热.同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热.待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热.同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热.待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使空气中的氧气充分反应.
(2)写出该实验中反应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(3)小强测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
①没有交替缓缓推动两个注射器活塞 ②读数时没有冷却至室温 ③加入铜丝量太少 ④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.(其它答案合理也可).
1.下列物质中,属于有机物的是( )
| A. | 二氧化碳 | B. | 一氧化碳 | C. | 碳酸氢钠 | D. | 尿素 |
5.20℃时50克水中最多可溶解5克A物质,20℃时100克水中最多可溶解10克B物质,则20℃时A和B的溶解度相比( )
| A. | A>B | B. | B>A | C. | A=B | D. | 无法比较 |
15.配置一定质量分数的硫酸铜溶液时,通常用不到的仪器是( )
| A. | 玻璃棒 | B. | 量筒 | C. | 温度计 | D. | 烧杯 |
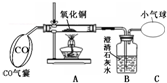 如图为一氧化碳与氧化铜反应的实验装置.请回答:
如图为一氧化碳与氧化铜反应的实验装置.请回答: