题目内容
5. 碱式氯化镁[Mg(OH)Cl]受热能分解,它分解后产物是什么?小科进行了探究.
碱式氯化镁[Mg(OH)Cl]受热能分解,它分解后产物是什么?小科进行了探究.【猜想】Mg(OH)Cl分解后产物可能有:Mg、MgCl2、MgO、HCl气体、H2O、Cl2.
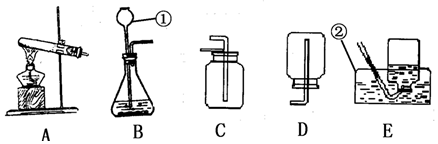
【实验一】取少量的Mg(OH)Cl放入大试管中,按如图所示装置进行实验,加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象.由此推知Mg(OH)Cl分解后产物中有HCl气体,无其他气体.
【实验二】取少量实验一的剩余固体于试管中,加入足量稀盐酸,没有气泡产生,由此推知Mg(OH)Cl分解后产物中没有Mg.
【实验三】再取少量实验一的剩余固体,加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生,由此推知Mg(OH)Cl分解后产物中没有MgCl2.
【结论】Mg(OH)Cl受热分解的化学反应方程式为Mg(OH)Cl$\frac{\underline{\;\;△\;\;}}{\;}$ MgO+HCl↑.
分析 【实验一】根据参加反应的物质及反应现象分析;
【实验二】根据镁能与稀盐酸反应生成氢气分析;
【实验三】根据氯离子与银离子结合生成白色沉淀分析;
【结论】根据反应物、生成物及质量守恒定律分析;
解答 解:【实验一】取少量的Mg(OH)Cl放入大试管中进行加热,加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象.由此可推知Mg(OH)Cl分解后产物中有氯化氢气体,氯离子与银离子结合生成了氯化银白色沉淀;故填:HCl;
【实验二】在Mg(OH)Cl分解后可能有的产物中只有Mg、MgCl2、MgO三种固体,Mg会与稀盐酸反应生成氢气,本实验中在剩余固体中加入足量稀盐酸,没有气泡产生,由此推知Mg(OH)Cl分解后产物中没有Mg;故填:Mg;
【实验三】若剩余固体中含有氯化镁,则加入AgNO3溶液后会有沉淀产生,加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生,由此推知Mg(OH)Cl分解后产物中没有MgCl2;故填:MgCl2;
【结论】由以上分析可知,Mg(OH)Cl受热分解生成氧化镁和氯化氢气体,反应的化学反应方程式为:Mg(OH)Cl $\frac{\underline{\;\;△\;\;}}{\;}$ MgO+HCl↑;故填:Mg(OH)Cl $\frac{\underline{\;\;△\;\;}}{\;}$ MgO+HCl↑;
点评 本题是实验推断题,熟练掌握各物质间的相互反应关系是解答问题的关键.

练习册系列答案
相关题目
20.关于H2O和H2O2的比较,不正确的是( )
| A. | 都含有氢、氧元素 | |
| B. | 都由氢、氧原子构成,结构相同 | |
| C. | 一定条件下都能分解产生氧气 | |
| D. | H2O是常见的溶剂,H2O2溶液可用于医疗消毒 |
13.关于化学反应“甲+乙→丙+丁”的分析正确的是( )
| A. | 若甲、乙各取10g混合,使其充分反应,则丙、丁质量的总和一定等于20g | |
| B. | 若丙为沉淀,则甲、乙中有一种物质是碱 | |
| C. | 若该反应为复分解反应,则生成物中一定有水 | |
| D. | 若乙和丁为单质,甲和丙为化合物,则该反应一定为置换反应 |
20.下列说法中,不正确的是( )
| A. | 用量筒量取一定量的水,读数时要平视液体凹形液面中央最低处 | |
| B. | 制作糖水时候,用玻璃棒搅拌可以加快糖的溶解 | |
| C. | 在用烧杯配制氢氧化钠溶液时,将氢氧化钠溶于水,会感觉烧杯壁比较热 | |
| D. | 因为氯化钠没有腐蚀性,所以可以直接在托盘天平上称量 |
10. 经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
查阅资料
①枸杞和合欢均可在轻度盐碱地中生存.
②盐碱地显碱性.
③该土样中的可溶性物质只含NaCl,CaCl2和Na2CO3.
探究过程
(1)甲组探究土样的酸碱度
具体操作是取土壤样品于烧杯中,加入蒸馏水搅拌、静置,用玻璃棒蘸取上层清液滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,由此得出,该土样的pH>7.
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸馏水,发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:只有氯化钠
猜想②:含有氯化钠、氯化钙
猜想③:含有氯化钠、碳酸钠
设计实验,继续探究:
反思与评价:
①通过交流,甲组认为乙组的方案一不太严谨,理由是若溶液中含有氯化钙,滴加AgNO3溶液和稀硝酸,也会产生白色沉淀.
②同学们对沉淀 CaCO3的来源展开了热烈的讨论.一致认为 CaCO3也可能来自土样本身.请解释土样中存在 CaCO3的原因在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀.
总结与提升:
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下建议你认为正确的是ac
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥.
 经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究查阅资料
①枸杞和合欢均可在轻度盐碱地中生存.
②盐碱地显碱性.
③该土样中的可溶性物质只含NaCl,CaCl2和Na2CO3.
探究过程
(1)甲组探究土样的酸碱度
具体操作是取土壤样品于烧杯中,加入蒸馏水搅拌、静置,用玻璃棒蘸取上层清液滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,由此得出,该土样的pH>7.
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸馏水,发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:只有氯化钠
猜想②:含有氯化钠、氯化钙
猜想③:含有氯化钠、碳酸钠
设计实验,继续探究:
| 验证猜想所用试剂 | 实验现象 | 实验结果 | |
| 方案一 | AgNO3溶液和稀硝酸 | 由白色沉淀生成 | 猜想①正确 |
| 方案二 | 碳酸钠溶液 | 无明显现象 | 猜想②不正确 |
| 方案三 | 稀盐酸 | 有气泡产生 | 猜想③正确 |
①通过交流,甲组认为乙组的方案一不太严谨,理由是若溶液中含有氯化钙,滴加AgNO3溶液和稀硝酸,也会产生白色沉淀.
②同学们对沉淀 CaCO3的来源展开了热烈的讨论.一致认为 CaCO3也可能来自土样本身.请解释土样中存在 CaCO3的原因在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀.
总结与提升:
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下建议你认为正确的是ac
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥.
17.一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
(1)通过上述实验可知,温度越高铁钉生锈速率越快(填“慢”或“快”);在酸性(填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
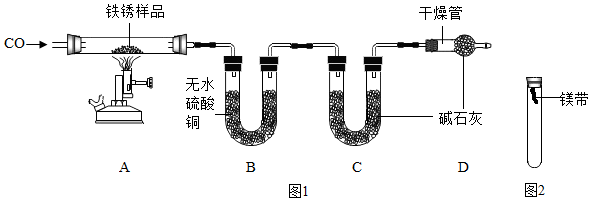
(2)请指出图1所示实验装置的一个明显缺陷:没有进行尾气处理.
(3)加热前,先通入CO一段时间,目的是排尽装置内的空气,防止发生爆炸.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有氢元素,从而推断出空气中的水参加了铁生锈反应.
【实验记录】
(5)根据上表数据推算,可确定铁锈的成分,用FexOy•nH2O表示,则n=4;若缺少D装置,x:y的值偏小(填“偏大”、“偏小”或“无影响”).
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2②水③CO2④O2和CO2⑤CO2和水⑥O2和水⑦O2、CO2和水
至少需要选用④⑤⑥⑦(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
| 实验图示 | 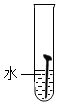 | 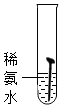 | 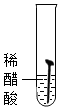 | 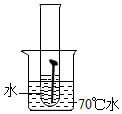 | 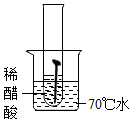 |
| 生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.

(2)请指出图1所示实验装置的一个明显缺陷:没有进行尾气处理.
(3)加热前,先通入CO一段时间,目的是排尽装置内的空气,防止发生爆炸.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有氢元素,从而推断出空气中的水参加了铁生锈反应.
【实验记录】
| 铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
| 反应前 | 23.2 | 232.4 | 198.2 |
| 反应后 | / | 239.6 | 211.4 |
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2②水③CO2④O2和CO2⑤CO2和水⑥O2和水⑦O2、CO2和水
至少需要选用④⑤⑥⑦(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2.
15.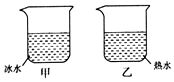 夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图所示,一会儿发现两只烧杯的杯壁上都有一部分出现小水珠,变得模糊了.针对这一现象,下列说法正确的是( )
夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图所示,一会儿发现两只烧杯的杯壁上都有一部分出现小水珠,变得模糊了.针对这一现象,下列说法正确的是( )
 夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图所示,一会儿发现两只烧杯的杯壁上都有一部分出现小水珠,变得模糊了.针对这一现象,下列说法正确的是( )
夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图所示,一会儿发现两只烧杯的杯壁上都有一部分出现小水珠,变得模糊了.针对这一现象,下列说法正确的是( )| A. | 甲、乙两杯都在内壁出现了水珠 | |
| B. | 甲、乙两杯都在外壁出现了水珠 | |
| C. | 甲杯的内壁出现了水珠,乙杯的外壁出现了水珠 | |
| D. | 甲杯的外壁出现了水珠,乙杯的内壁出现了水珠 |
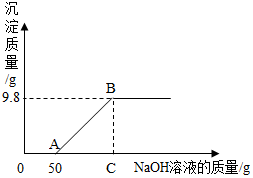 现有硫酸和硫酸铜的混合溶液200g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀质量与所加入的氢氧化钠溶液的质量关系如图所示.求:
现有硫酸和硫酸铜的混合溶液200g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀质量与所加入的氢氧化钠溶液的质量关系如图所示.求: