题目内容
18.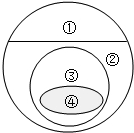 如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )
如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )| A. | ①单质 ④含氧化合物 | B. | ②化合物 ③氧化物 | ||
| C. | ①单质 ③化合物 | D. | ②化合物 ④氧化物 |
分析 物质包括混合物和纯净物,纯净物包括单质和化合物,化合物包括含氧化合物,含氧化合物包括氧化物.
解答 解:由图中信息可知,①代表单质,②代表化合物,③代表含氧化合物,④氧化物.
故选:D.
点评 本题主要考查物质的分类,只要掌握了物质的分类方法,解答起来比较简单.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
8.小刚同学在实验室中用过氧化氢制取了氧气,实验又展开了下列思考与探究:
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
由表中数据可以得到相应的结论是二氧化锰的量会影响过氧化氢的反应速率,且在一定范围内,二氧化锰的量越大,反应速率越快.
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
由表中数据可以得到的结论是过氧化氢溶液的溶质质量分数越大,化学反应速率越快.
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量/克 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体所用时间/秒 | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..
6.同学们填写的“毕业生登记表”需要( )
| A. | 碳素笔 | B. | 圆珠笔 | C. | 红墨水笔 | D. | 蓝墨水笔 |
3.向装有等量水的A、B、C三个烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图1所示,如图2表示甲、乙两物质的溶解度曲线.下列说法中正确的是( )

| A. | 三个烧杯中形成的溶液都是饱和溶液 | |
| B. | 图中表示NaNO3溶解度曲线的是乙 | |
| C. | B和C烧杯中都放有25g NaNO3固体,所以溶液溶质质量分数相等 | |
| D. | 分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,所得的溶质质量:乙<甲 |
7.如表是某同学用多种方法鉴别物质的情况,其中两种方法都正确的是( )
| 选项 | 需要鉴别的物质 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| A | 稀盐酸和稀硫酸 | 滴加紫色石蕊溶液 | 滴加氯化钡溶液 |
| B | 硫酸铵和磷矿粉 | 加入足量水 | 观察颜色 |
| C | 硝酸铵和硝酸钾 | 加入熟石灰、研磨 | 滴加水 |
| D | 稀烧碱溶液与石灰水 | 滴加石蕊溶液 | 加入氯化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
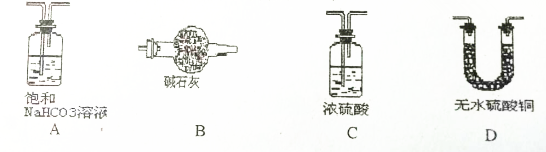

 某同学利用“多米诺骨牌”效应,设计了如下气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到B中导管口有气泡冒出,请看图回答问题:
某同学利用“多米诺骨牌”效应,设计了如下气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到B中导管口有气泡冒出,请看图回答问题: 如图为测定空气中氧气的含量的实验装置图.
如图为测定空气中氧气的含量的实验装置图.