题目内容
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
①制备氧化铜并检验产物,装置如下图所示(省略夹持仪器):
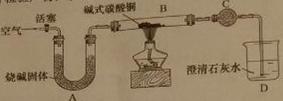
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
B中发生反应的化学方程式为: 1 Cu2(OH)2CO3 2CuO + 1 H2O + 1 CO2↑
2CuO + 1 H2O + 1 CO2↑
 请在 中填入配平后的系数 。
请在 中填入配平后的系数 。
C中试剂是 。A的作用是吸收空气中的 ,防止对产物检验造成干扰。选择t3时停止加热的理由是 。
② 一定量碳粉还原①中制得的氧化铜并检验产物,装置如下图所示:
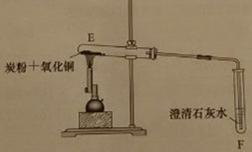
实验过程中,观察到F中溶液变浑浊,E中的现象是 。
反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是 。
③ 分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因。
【答案】
①1、2、1、1 无水硫酸铜 水蒸气和二氧化碳 固体质量不再减少,证明碱式碳酸铜已经完全分解
②黑色粉末变成红色 F中液体通过导管流入E中,造成试管炸裂
③不能确定碳粉还原氧化铜的生成物中是否有二氧化碳。因为可能有①中未分解的碱式碳酸铜,在实验②中分解,产生二氧化碳气体,干扰对碳粉还原氧化铜反应生成物的判断。
【解析】①依据质量守恒定律,反应前后各原子的种类和数目不变,可以确定Cu2(OH)2CO3、CuO、H2O、CO2前的化学计量数分别是1、2、1、1;实验产生二氧化碳和水蒸气两种气体,C、D中的试剂分别用于验证反应产物,D中的澄清石灰水用于检验反应是否产生二氧化碳,则D中的试剂用于检验反应是否产生水,实验室中常用无水硫酸铜检验水的存在(无水硫酸铜遇水变成蓝色);为了避免玻璃管内空气中的二氧化碳和水蒸气对实验产物的检验造成干扰,需用A中的氢氧化钠固体将先空气中的二氧化碳和水蒸气除去,然后用除去二氧化碳和水蒸气的空气将玻璃管中的空气排净;只有确定玻璃管中的固体在加热过程中质量不再减小,才能证明碱式碳酸铜已完全分解;②碳粉和氧化铜在高温条件下能够发生化学反应:C+2CuO2Cu+CO2↑,当F中的澄清石灰水变浑浊,说明反应已经发生,即黑色的氧化铜与碳粉反应生成红色的金属铜,则E中一定能够观察到黑色粉末变成红色;实验结束后,应先将导管从试管中移出,再撤走酒精喷灯,若反应完全后仅撤走酒精喷灯停止加热,则会导致F中液体通过导管流入E中,使试管骤冷而炸裂;若①中省略步骤三,①可能有中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体也会使F中的澄清石灰水变浑浊,因此将无法确定该二氧化碳是否为炭粉还原氧化铜生成的二氧化碳,干扰对炭粉还原氧化铜反应生成物的判断。

近年来,建筑装潢装饰材料进入家庭。调查发现,经装修的居室中有装潢装饰材料缓慢释放出的化学物质浓度过高,影响人体健康。这些化学物质中最常见的是( )
A.CO B.SO2
C.甲醛等有机物蒸气  D.臭氧
D.臭氧
某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们提出了如下假设:
【猜 想】猜想一:没有变质; 猜想二:部分变质; 猜想三: ① 。
【查阅资料】Na2CO3溶液呈碱性。
【进行实验】对猜想二进行验证。
| 实验步骤 | 实验现象 | 结论 |
| 1. 取少许该溶液于试管中,滴 入适量的 ② 溶液。 | ③ | 猜想二正确 |
| 2.静置上述溶液,取上层清液少许于另一支试管中,滴入几滴 ④ 溶液 | ⑤ |
写出现象③的化学方程式 ⑥ 。
【反 思】氢氧化钠溶液必须密封保存。
氢氧化钠溶液变质的原因(用化学方程表示) ⑦ 。
化学兴趣小组设计的创新实验是“火龙生字”。在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)。用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(间图2)。在场的同学对此产生了浓厚的兴趣,并进行了如下探究:
【提出问题】为甚附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于生成的是什么气体,四位同学有如下猜想:
甲:二氧化氮;乙:氮气;丙:氧气;丁:氢气。
同学丙指出不可能是二氧化氮、氢气,理由是: ; 。
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是:
,观察到的现象是 ,说明同学丙的猜想正确。
硝酸钾分解的化学方程式是 :
【解释与结论】白纸上写过字的地方更容易燃烧的原因是: 。
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
你对上述问题的解释: 。
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 ▲ 、 ▲ 。
(2)可以通过比较 ▲ 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 ▲ 。




 碳的化学方程式 ② 。
碳的化学方程式 ② 。 验 ③ (填“能”或“不能”)证明她的猜想,理由是④ 。
验 ③ (填“能”或“不能”)证明她的猜想,理由是④ 。