题目内容
5.某同学欲选用下列几组实际探究Al、Fe、Cu三种金属的活动性顺序,其中不能达到目的是( )| A. | Fe、Cu、Al(SO4)3溶液 | B. | Al、Cu、FeSO4溶液 | ||
| C. | Fe、Al2(SO4)3溶液、CuSO4溶液 | D. | Al、Fe、Cu、稀H2SO4 |
分析 根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断,通过分析方案所能得到的结论,确定是否能得出Mg、Fe、Cu三种金属的活动性顺序.
解答 解:A、铁、铜与Al(SO4)3溶液均不反应,说明了活动性铝>铁,铝>铜,但无法确定铁和铜的活动性强弱,故该方案不合理.
B、铜与FeSO4溶液不反应,说明了活动性铁>铜;铝与FeSO4溶液反应置换出铁,说明了活动性铝>铁,由此可得的三种金属活动性铝>铁>铜,故该方案合理.
C、铁与CuSO4溶液反应置换出铜,说明了活动性铁>铜;铁与Al2(SO4)3溶液不反应,说明了活动性铝>铁,由此可得的三种金属活动性铝>铁>铜.故该方案合理
D、铝、铁与稀H2SO4反应生成了氢气,但铝反应剧烈,说明了活动性铝>铁;铜与稀H2SO4不反应说明铜位于氢的后面,由此可得的三种金属活动性是铝>铁>铜,故该方案合理.
故选A.
点评 本题难度不是很大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
15.如图所示为实验室常见的气体制备、净化、收集和性质实验的部分仪器.试根据题目要求,回答下列问题:
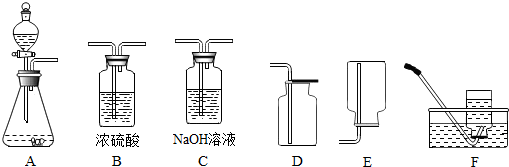
(1)小欣同学用过氧化氢溶液与二氧化锰为原料,在实验室制取并收集一瓶干燥的氧气.
①该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②所选仪器的连接顺序为ABD(填写仪器序号字母).
③反应完毕,从混合物中分离出二氧化锰的最佳方案是溶解、过滤、洗涤、干燥.
(2)某实验小组的同学用锌和稀硫酸反应制取氢气,并用来测定某氧化铜样品的纯度,其实验装置及实验数据如图表所示.(已知:样品中杂质不参与反应,H2+CuO═Cu+H2O,设各步均完全反应.)
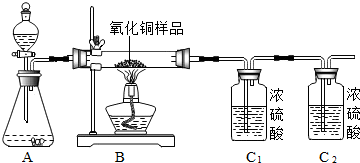
①甲同学通过测量反应前、后装置B中固体的质量变化,可计算出氧化铜样品的纯度为80.0%(数据精确至0.1%).
②乙同学通过测量反应前、后装置C1的质量变化,计算出该氧化铜样品的纯度为88.9%.试分析乙同学计算结果存在误差的原因:生成的氢气中混有的水蒸气.
请你对上图实验装置提出具体的改进措施:将C2装置放在AB装置之间.

(1)小欣同学用过氧化氢溶液与二氧化锰为原料,在实验室制取并收集一瓶干燥的氧气.
①该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②所选仪器的连接顺序为ABD(填写仪器序号字母).
③反应完毕,从混合物中分离出二氧化锰的最佳方案是溶解、过滤、洗涤、干燥.
(2)某实验小组的同学用锌和稀硫酸反应制取氢气,并用来测定某氧化铜样品的纯度,其实验装置及实验数据如图表所示.(已知:样品中杂质不参与反应,H2+CuO═Cu+H2O,设各步均完全反应.)

| 装置B中固体质量 | 装置C1的质量 | |
| 反应前 | 10.0克 | 150.8克 |
| 反应后 | 8.4克 | 152.8克 |
②乙同学通过测量反应前、后装置C1的质量变化,计算出该氧化铜样品的纯度为88.9%.试分析乙同学计算结果存在误差的原因:生成的氢气中混有的水蒸气.
请你对上图实验装置提出具体的改进措施:将C2装置放在AB装置之间.
17.下列说法不正确的是( )
| A. | 食品包装充氮气以防腐 | B. | 混合施用氯化铵和草木灰 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 把石墨制成电池中的电极 |
14.二甲醚(C2H6O)是一种重要的化工原料,下列关于二甲醚的说法错误的是( )
| A. | 由3种元素组成 | B. | 相对分子质量为9 | ||
| C. | 碳、氢、氧元素质量比为12:3:8 | D. | 碳元素的质量分数约为52.2% |
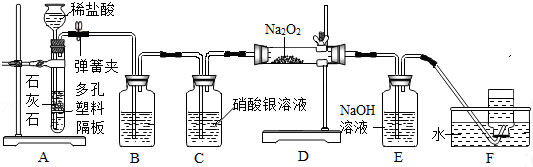


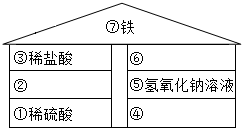 你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应“来堆砌物质,其中有碳酸钠、二氧化碳、硫酸铜溶液这三种物质找不到自己的位置了,请你帮忙:
你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应“来堆砌物质,其中有碳酸钠、二氧化碳、硫酸铜溶液这三种物质找不到自己的位置了,请你帮忙: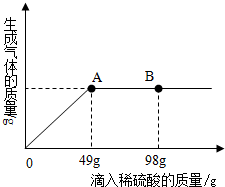 在一烧杯中盛有22.4gNa2CO3和Na2SO4组成的固体混合物,加入84克水使Na2CO3和Na2SO4全部溶解.向其中逐渐滴加溶质质量分数为20%的稀硫酸.生成气体的总质量与所滴入稀硫酸的质量关系曲线如下图所示,请根据题意回答问题:
在一烧杯中盛有22.4gNa2CO3和Na2SO4组成的固体混合物,加入84克水使Na2CO3和Na2SO4全部溶解.向其中逐渐滴加溶质质量分数为20%的稀硫酸.生成气体的总质量与所滴入稀硫酸的质量关系曲线如下图所示,请根据题意回答问题: