题目内容
16.有一种生氧防毒面具,它由面罩、生氧罐、呼气管和吸气管等组成.在生氧罐中有淡黄色的粉末过氧化钠(Na2O2).某化学兴趣小组在实验室中探究该面具的防毒原理.查阅资料:(1)2Na2O2+2CO2═2Na2CO3+O2 (2)2Na2O2+2H2O═4NaOH+O2↑
(3)2Na2O2+4HCl═4NaCl+2H2O+O2↑ (4)Na2CO3+CO2+H2O═2NaHCO3
实验设计:
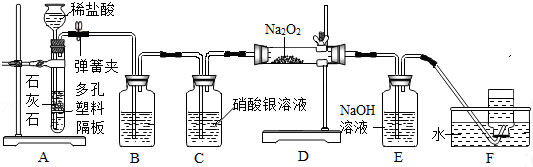
请回答下列问题:
(1)装置A中发生反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O,利用装置A制取CO2的优点是可以控制反应的发生与停止.
(2)装置B中的物质是B(填序号).
A.NaOH溶液 B.饱和NaHCO3溶液 C.Na2CO3溶液
(3)装置C的作用是证明HCl已除尽或检验HCl是否已除尽,装置E中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O,检验装置F中收集到的气体方法是将带火星的木条伸入瓶内,若复燃,证明是氧气.
(4)小亮为进一步探究反应后装置D中固体的成分,进行了如下实验:

请完成部分实验报告:
操作Ⅰ中加水溶解无气泡,说明固体中无Na2O2,操作Ⅱ中加入足量BaCl2溶液的作用是证明并除尽Na2CO3或除尽Na2CO3或除去Na2CO3,根据实验现象判断反应后装置D中固体的化学式为NaOH和Na2CO3.
实验结论:该防毒面具利用人体呼出的气体和氧化钠反应,产生氧气,供人呼吸.
意外探究:小亮同学向上述红色的溶液中意外加入氢氧化钠固体,溶解,发现红色褪去,加水,红色又出现,红色褪去的原因估计是NaOH溶液浓度太大.
分析 (1)据反应原理书写方程式;并据装置特点分析解答;
(2)根据装置B的作用是除去氯化氢解答;
(3)根据装置C的作用是证明HCl已除尽或检验HCl是否已除尽解答;
(4)根据2Na2O2+2H2O═4NaOH+O2↑可知,操作Ⅰ中加水溶解无气泡,说明固体中无Na2O2;BaCl2溶液和碳酸钠反应解答;
解答 解:
(1)石灰石的主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;利用装置A制取CO2的优点是可以控制反应的发生与停止;
(2)装置B的作用是除去氯化氢;
A.NaOH溶液可以与氯化氢、二氧化碳都反应,错误;
B.饱和NaHCO3溶液只与氯化氢,正确;
C.Na2CO3溶液可以与氯化氢、二氧化碳都反应,错误;
(3)硝酸银和氯化氢反应,生成氯化银白色沉淀,装置C的作用是证明HCl已除尽或检验HCl是否已除尽;装置E中发生反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;检验装置F中收集到的气体方法是将带火星的木条伸入瓶内,若复燃,证明是氧气;
(4)由2Na2O2+2H2O═4NaOH+O2↑可知,操作Ⅰ中加水溶解无气泡,说明固体中无Na2O2;操作Ⅱ中加入足量BaCl2溶液,产生白色沉淀,则证明并除尽Na2CO3并除尽Na2CO3;根据滤液中加酚酞,溶液变红,说明溶液中用氢氧化钠,实验现象判断反应后装置D中固体的化学式为NaOH和Na2CO3;
小亮同学向上述红色的溶液中意外加入氢氧化钠固体,溶解,发现红色褪去,加水,红色又出现,红色褪去的原因估计是NaOH溶液浓度太大.
答案:
(1)CaCO3+2HCl═CaCl2+CO2↑+H2O; 发生与停止;
(2)B;
(3)证明HCl已除尽或检验HCl是否已除尽;CO2+2NaOH═Na2CO3+H2O;将带火星的木条伸入瓶内,若复燃,证明是氧气;
(4)Na2O2; 证明并除尽Na2CO3或除尽Na2CO3或除去Na2CO3 (只答证明有Na2CO3不给分);NaOH和Na2CO3; NaOH溶液浓度太大.
点评 该题根据查阅资料提供的信息并结合实验步骤和现象解决问题.主要考查读题能力,能把题目所给信息与所学知识进行牵连.知道性质决定用途,用途体现性质.

| A. | 氧气作燃料 | B. | 干冰用于人工降雨 | ||
| C. | 氢氧化钠用于改良酸性土壤 | D. | 甲醛用于泡发鱿鱼等水产品 |
| A. | 2个氢分子2H | B. | 4个水分子 4H2O | C. | 钴元素CO | D. | 3个氧原子O3 |
| A. | 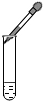 滴加液体 | B. | 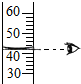 量取液体体积读数 | ||
| C. | 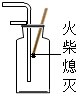 二氧化碳验满 | D. | 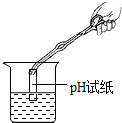 测定溶液的pH |
| A. | 玻璃杯 | B. | 塑料袋 | C. | 不锈钢锅 | D. | 纯羊毛绒 |
| A. | Fe、Cu、Al(SO4)3溶液 | B. | Al、Cu、FeSO4溶液 | ||
| C. | Fe、Al2(SO4)3溶液、CuSO4溶液 | D. | Al、Fe、Cu、稀H2SO4 |
