题目内容
根据如图所示实验,回答以下问题.
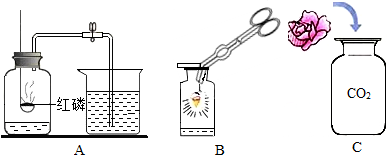
(1)A为测定空气中氧气含量的实验装置,有关反应的化学方程式为 ;通过该实验可得出氧气约占空气总体积的 的结论.
(2)集气瓶B中的现象:铁丝在氧气中剧烈燃烧, ,放出大量的热,有黑色固体生成.该反应的化学方程式为 .
(3)取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入集气瓶C中,观察到的现象是 .

(1)A为测定空气中氧气含量的实验装置,有关反应的化学方程式为
(2)集气瓶B中的现象:铁丝在氧气中剧烈燃烧,
(3)取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入集气瓶C中,观察到的现象是
考点:空气组成的测定,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:空气与水,碳单质与含碳化合物的性质与用途
分析:(1)根据测定空气中氧气含量实验发生的反应及结论分析回答;
(2)根据铁丝在氧气中燃烧的现象及发生的反应分析回答;
(3)二氧化碳能与水化合生成碳酸,碳酸显酸性,能使紫色的石蕊试液变红色.
(2)根据铁丝在氧气中燃烧的现象及发生的反应分析回答;
(3)二氧化碳能与水化合生成碳酸,碳酸显酸性,能使紫色的石蕊试液变红色.
解答:解:(1)在测定空气中氧气含量时,红磷燃烧生成了五氧化二磷,反应的化学方程式为:4P+5O2
2P2O5;通过该实验可得出氧气约占空气总体积的
的结论.
(2)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,有黑色固体生成.该反应的化学方程式为:3Fe+2O2
Fe3O4.
(3)由于二氧化碳能与水化合生成碳酸,碳酸显酸性,能使紫色的石蕊试液变红色.所以,观察到的现象是:小花干燥的一半无变化,喷水的一半变为红色.
故答为:(1)4P+5O2
2P2O5,
;(2)火星四射,3Fe+2O2
Fe3O4.(3)小花干燥的一半无变化,喷水的一半变为红色.
| ||
| 1 |
| 5 |
(2)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,有黑色固体生成.该反应的化学方程式为:3Fe+2O2
| ||
(3)由于二氧化碳能与水化合生成碳酸,碳酸显酸性,能使紫色的石蕊试液变红色.所以,观察到的现象是:小花干燥的一半无变化,喷水的一半变为红色.
故答为:(1)4P+5O2
| ||
| 1 |
| 5 |
| ||
点评:本考点主要考查了测定空气中氧气含量、铁丝的燃烧和二氧化碳的化学性质,特别是二氧化碳的化学性质,是中考的重点内容,一定要认真练习书写,综合把握.

练习册系列答案
相关题目
测定空气中氧气体积分数的实验,一般选择下列的( )来除去氧气.
| A、镁条 | B、硫粉 | C、蜡烛 | D、红磷 |
 测定空气中氧气含量的实验装置如图所示,实验步骤如下:
测定空气中氧气含量的实验装置如图所示,实验步骤如下: 兴趣小组为了测定“碳还原氧化铜”实验中所用的氧化铜样品中的CuO含量,进行如下实验:用过量的稀盐酸溶解5g样品(杂质不与盐酸反应且不溶于水),过滤,取100g滤液,向其中加入NaOH溶液,所得实验数据如图:
兴趣小组为了测定“碳还原氧化铜”实验中所用的氧化铜样品中的CuO含量,进行如下实验:用过量的稀盐酸溶解5g样品(杂质不与盐酸反应且不溶于水),过滤,取100g滤液,向其中加入NaOH溶液,所得实验数据如图: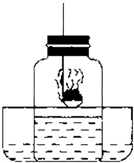 我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.
我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.