题目内容
18.某同学用纯净、干燥的一氧化碳做还原氧化铜的实验,因一氧化碳中混有少量二氧化碳,还要防止反应后多余的一氧化碳污染空气,他准备了甲、乙、丙、丁四个装置(丙装置中的浓硫酸可吸收水蒸气),试回答下列问题:
(1)装置丙中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳;浓硫酸的作用是干燥一氧化碳.
(2)实验进行时,各装置口的连接顺序为:A-E-D-F-G-B.
(3)由于C处放出的气体含有一氧化碳,因而应进行将尾气点燃(或收集)处理.
分析 (1)根据氢氧化钠的性质以及浓硫酸的吸水性来分析;
(2)一氧化碳中混有少量二氧化碳,故需要先除去二氧化碳再进行实验,可用氢氧化钠溶液吸收二氧化碳,再通过浓硫酸干燥,然后通过氧化铜进行实验,检验二氧化碳用澄清石灰水并处理尾气;
(3)尾气中含有一氧化碳,一氧化碳有毒,不能直接排放到空气中,需要进行尾气处理,一般可采用点燃或用气球收集的方法.
解答 解:(1)二氧化碳能与氢氧化钠反应生成碳酸钠和水,所以氢氧化钠溶液可以吸收混合气体中的二氧化碳,浓硫酸具有吸水性,可以吸收一氧化碳中的水蒸气;故填:吸收混合气体中的二氧化碳;干燥一氧化碳;
(2)根据题目要求,需要先除去二氧化碳再进行干燥,然后还原氧化铜的实验,最后进行尾气处理,所以装置连接顺序为:A→E→D→F→G→B;故填:E;D;F;B;
(3)尾气中含有一氧化碳和二氧化碳,通过石灰水后,二氧化碳被吸收,因为一氧化碳有毒,会污染空气,所以要先处理再排放,可采用点燃或用气球收集的方法.故填:一氧化碳;将尾气点燃(或收集).
点评 本题考查一氧化碳还原氧化铜的实验装置及相关问题,属于课本基本实验的延伸,难度不大,容易出错的是(2)装置的连接,要注意的是吸收二氧化碳用氢氧化钠,检验二氧化碳用澄清石灰水.

| A. | Cu | B. | Ag | C. | Cu和Ag | D. | Fe和Cu |
某校化学兴趣小组的同学们帮助实验老师整理化学药品室时,发现两个未贴标签的试剂瓶中分别存放银白色金属片.到底它们是哪两种金属?请同学们设计实验方案对这两种金属X和Y的金属活动性顺序进行实验探究.
(1)进行实验,获得结论.完成好如下实验报告,并回答后续有关问题.
实验步骤 | 实 验 现 象 | 结 论 |
分别把这两种金属放入 ______ 溶液中,观察. | 金属Y表面无明显变化;金属X的表面有大量气泡冒出.将燃着的木条放在金属X的试管口,气体燃烧. | 金属活动性顺序: _________ |
(2)在进行上述实验之前,实验老师只知道X、Y可能是铝、银中的各一种,则根据实验结果说明X是______ ,反应的化学方程式为 _____________________。
(3)小明同学提出,还可以用其它方法证明X、Y的活动性。请你用化学方程式表示(应有明显的实验现象)_________________________________。

 ”“
”“ ”分别表示两种不同的原子,其中属于单质的是AB;属于化合物的是D;属于混合物的是C.
”分别表示两种不同的原子,其中属于单质的是AB;属于化合物的是D;属于混合物的是C.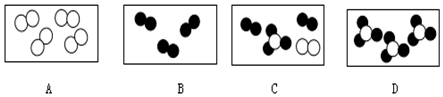
 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小科突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小科又进行了如下实验:
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小科突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小科又进行了如下实验: