题目内容
18.今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气.先向气体发生装置中加入一定量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(1)共制得氢气0.2g.
(2)实验所用稀硫酸中溶质的质量分数.(写出计算过程)
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据表中提供的数据和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)共制得氢气质量为:0.08g+0.08g+0.04g=0.2g,
故填:0.2.
(2)由表中数据可知,第1次20g稀硫酸中的硫酸完全反应,设20g稀硫酸中硫酸质量为x,
Zn+H2SO4═ZnSO4+H2↑,
98 2
x 0.08g
$\frac{98}{x}$=$\frac{2}{0.08g}$,
x=3.92g,
实验所用稀硫酸中溶质的质量分数为:$\frac{3.92g}{20g}$×100%=19.6%,
答:实验所用稀硫酸中溶质的质量分数为19.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.下列实验操作正确的是( )
| A. | 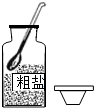 取用固体药品 | B. | 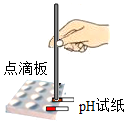 测溶液的pH 测溶液的pH | C. | 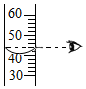 量取40mL溶液 | D. | 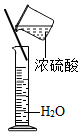 稀释浓硫酸 |
9.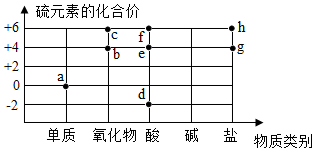 图中字母代表含硫元素的物质,下列判断错误的是( )
图中字母代表含硫元素的物质,下列判断错误的是( )
 图中字母代表含硫元素的物质,下列判断错误的是( )
图中字母代表含硫元素的物质,下列判断错误的是( )| A. | 物质a在纯氧中燃烧可以生成物质b | B. | 物质c是二氧化硫 | ||
| C. | 物质d中硫元素的化合价为-2价 | D. | 物质d、e和f中一定都含有氢元素 |
6.“青山绿水就是金山银山”.为了实现这一目标,菏泽市多地已经开始实行电动公交出行,推广太阳能路灯,升级改造燃煤锅炉.你认为下列做法与这一理念不相符的是( )
| A. | 工业废水经处理达标后排放 | |
| B. | 尽量不使用一次性塑料袋购物,减少“白色污染” | |
| C. | 植树造林,增大绿化面积 | |
| D. | 加高燃煤锅炉烟囱,将废气排到高空 |
13.下列实验方案设计不合理的是( )
| 实验目的 | 实验方案 | |
| A | 除去二氧化碳中的一氧化碳 | 将气体通入氢氧化钠溶液 |
| B | 检验甲烷中是否含有氢元素 | 点燃,在火焰上方罩一干冷的烧杯,观察现象 |
| C | 区别棉线和羊毛线 | 分别灼烧,闻气味 |
| D | 除去食盐中的泥沙 | 溶解、过滤、蒸发 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
2.正确的化学实验操作对实验结果、人身安全非常重要.下列实验操作正确的是( )
| A. |  取用液体药品 | B. |  检测溶液的pH值 | ||
| C. |  稀释浓硫酸 | D. |  检验甲烷燃烧有CO2生成 |
6.实验室中有一瓶含有少量氯化钠和不可溶性杂质的硫酸钠样品.某化学兴趣小组对该样品成分进行定量测定,甲、乙、丙三位同学分别称取一定质量的样品放入烧杯中,溶入足量水后过滤得到滤液;再向滤液中加入一定质量的氯化钡溶液,充分反应后过滤,将沉淀洗涤、干燥并称量.相关实验数据记录如下:
请回答下列问题:
计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
| 称量项目 | 甲 | 乙 | 丙 |
| 所取样品的质量/g | 15 | 15 | 20 |
| 加入氯化钡溶液的质量/g | 150 | 100 | 100 |
| 反应后所得沉淀的质量/g | 23.3 | 23.3 | 23.3 |
计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
7.氮气在物质分类中属于( )
| A. | 单质 | B. | 化合物 | C. | 氧化物 | D. | 混合物 |
