题目内容
13.能源是人类社会发展的基础,化石燃料是目前人类应用最广泛的能源物质,请回答下列问题:(1)目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和天然气,液化天然气(LNG)是目前正在推广使用的公交车燃料,它具有燃烧效率高、污染小的优点.写出天然气主要成分完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳在高温下与水的反应,其微观示意图如下所示:
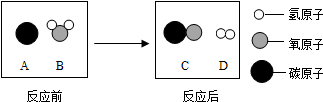
通过观察图你能获得的信息是(写出两条即可):
①化学反应前后原子的种类不变;②化学反应前后原子的数目不变.
写出该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(3)为减少CO2的排放,人们积极寻找不含碳元素的燃料,经研究发现NH3气在氧气中燃烧的产物没有污染,生成水和空气中含量最多的一种气体,且释放大量的热,有一定应用前景.则NH3在氧气中燃烧的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2.
分析 (1)天然气的主要成分是甲烷,甲烷燃烧生成水和二氧化碳;
(2)根据反应的微观示意图及质量守恒定律分析解答;
(3)根据氨气和氧气反应生成水和氮气进行解答.
解答 解:
(1)甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)由反应的微观示意图及质量守恒定律可知,化学反应前后原子的种类不变,化学反应前后原子的数目不变;碳在高温下与水的反应生成一氧化碳和氢气,该反应的化学方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2
(3)氨气在纯净氧气中燃烧,生成空气中含量最多的气体是氮气,一种常温下为液体的氧化物为水,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2.
答案:
(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
(2)①化学反应前后原子的种类不变;②化学反应前后原子的数目不变;C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2
(3)4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2.
点评 本题考查了化学与生活的知识,完成此题,可以依据已有的知识进行.书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
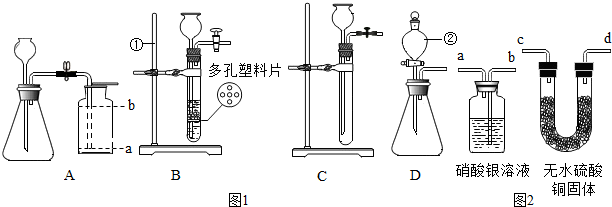
3. 如图所示,打开止水夹,将液体A滴入试管②中与固体B接触,试管①中没入水面下的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
如图所示,打开止水夹,将液体A滴入试管②中与固体B接触,试管①中没入水面下的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
 如图所示,打开止水夹,将液体A滴入试管②中与固体B接触,试管①中没入水面下的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
如图所示,打开止水夹,将液体A滴入试管②中与固体B接触,试管①中没入水面下的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )| A. | 水和生石灰 | B. | 稀盐酸和铜 | C. | 水和氢氧化钠 | D. | 稀硫酸和铝 |
4.某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行);①通过赤热的炭层后,恢复到原状态,气体分子总数不变;②通过灼热的氧化铁时,红色固体消失;③通过白色CuS04粉末时,粉末变成蓝色晶体;④通入澄清石灰水中,石灰水变浑浊.下列判断正确的是( )
| A. | 原混合气体中只含有CO和H2 | |
| B. | 原混合气体中一定含有CO2、CO和H2 | |
| C. | 原混合气体中一定含有H2和CO2,可能含有CO | |
| D. | 原混合气体中一定没有CO2,可能含有H2和CO |
1.表是元素周期表的一部分,请你根据表回答问题:
(1)根据表回答问题
①钠的相对原子质量是22.99.
②表中,金属元素有5种.
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
①该元素的原子的核电荷数为16,该原子的最外层电子数为6.
②图乙所示粒子的符号为S2-.

| 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 11 Na 钠 2 2.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 1 8 Ar 氩 29.95 |
①钠的相对原子质量是22.99.
②表中,金属元素有5种.
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
①该元素的原子的核电荷数为16,该原子的最外层电子数为6.
②图乙所示粒子的符号为S2-.

8.实验是化学研究的主要手段,下列化学实验操作正确的是( )
| A. |  向试管中滴加液体 | B. |  过滤 | ||
| C. |  闻气味 | D. |  点燃酒精灯 |
18.铬(Cr)为不锈钢主要的添加元素,含量一般在12%以上.铬的表面生成一薄层致密的氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:
(1)铁生锈的主要条件是铁与氧气和水直接接触.
(2)不锈钢是一种合金(填“合成材料”或“合金”)
(3)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
①上述三种金属的活动性由强到弱的顺序是Mg、Cr、Cu.
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
(1)铁生锈的主要条件是铁与氧气和水直接接触.
(2)不锈钢是一种合金(填“合成材料”或“合金”)
(3)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
5.向下列物质中分别加入足量的蒸馏水,搅拌后能形成无色溶液的是( )
| A. | 面粉 | B. | 氯化亚铁 | C. | 食盐 | D. | 食用油 |
2.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 分子是构成物质的微粒,物质都是由分子构成的 | |
| B. | 氧化物一定含氧元素,含氧元素的物质一定是氧化物 | |
| C. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| D. | 酸性较强的溶液能使石蕊溶液变红,能使石蕊溶液变红的溶液一定呈酸性 |