题目内容
18.对下列事实的微观解释正确的是( )| A. | 冰融化成水--分子种类发生改变 | |
| B. | 分离液态空气制取氧气--分子可以再分 | |
| C. | 压缩的乒乓球放入热水中重新鼓起--温度升高,分子的体积增大 | |
| D. | NaOH溶液、Ca(OH)2溶液均显碱性--溶液中都含有OH- |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,逐项进行分析判断即可.
解答 解:A、冰融化成水是物理变化,在物理变化中分子本身没有变化,分子种类没有改变,故错误;
B、分离液态空气制氧气是物理变化,在物理变化中分子本身没有变化,故错误;
C、由于分子间有间隔,受热时间隔变大,所以,压瘪的乒乓球放入热水中重新鼓起,分子的体积不变,故错误;
D、NaOH溶液、Ca(OH)2溶液均显碱性是因为溶液中都含有OH-,故正确.
故选D.
点评 本题难度不大,掌握利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
9.市场上有“高钙牛奶”、“加碘食盐”等商品,这里的“钙、碘“应理解为( )
| A. | 原子 | B. | 分子 | C. | 元素 | D. | 单质 |
3.下列图象能正确反映其对应关系的是( )
| A. |  加热一定质量的氯酸钾和二氧化锰的混合物制氧气 | |
| B. |  等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应 | |
| C. |  一定温度下,向一定质量的饱和石灰水中加入氧化钙 | |
| D. |  向一定量的氢氧化钡溶液中不断加入稀硫酸 |
10. 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣,在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣,在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
老师提示:
Ⅰ.电解饱和食盐水生成烧碱、氢气和氯气,则其反应的化学方程式为NaOH+HCl═NaCl+H2O.
Ⅱ.可以忽略其他可能发生的反应对以下实验的影响.
Ⅲ.氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2═Ma(OH)2↓+2NaCl
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
(2)写出氢氧化钠与稀盐酸反应的化学方程式:NaOH+HCl═NaCl+H2O.
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
乙组同学按如图所示的实验步骤进行实验:
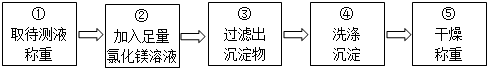
(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是Mg(OH)2(填化学式).
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣,在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣,在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.老师提示:
Ⅰ.电解饱和食盐水生成烧碱、氢气和氯气,则其反应的化学方程式为NaOH+HCl═NaCl+H2O.
Ⅱ.可以忽略其他可能发生的反应对以下实验的影响.
Ⅲ.氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2═Ma(OH)2↓+2NaCl
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
| 向待测液中滴加几滴酚酞试液 | 酚酞试液变红色 | 待测液呈碱性,表明含有氢氧化钠. |
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
乙组同学按如图所示的实验步骤进行实验:

(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是Mg(OH)2(填化学式).
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
7.下列各组离子在溶液中可以大量共存的是( )
| A. | Ba2+、NO3-、NH4+ | B. | H+、K+、CO32- | C. | Ca2+、CO32-、Cl- | D. | OH-、Na+、Cu2+ |
8.空气是一种宝贵的自然资源,从分离空气的成分中不能得到的气体是( )
| A. | 用作医疗急救的氧气 | B. | 用作霓虹灯中填充气的稀有气体 | ||
| C. | 用作食品防腐剂的氮气 | D. | 用作清洁燃料的氢气 |
 如图是化学园地中一张表示物质间反应关系的卡片图(“-”表示相连的两种物质能够在溶液体系中发生化学反应),其中A、B、C三处的卡片尚未粘贴.请你思考一种粘贴方案,并回答下列问题:
如图是化学园地中一张表示物质间反应关系的卡片图(“-”表示相连的两种物质能够在溶液体系中发生化学反应),其中A、B、C三处的卡片尚未粘贴.请你思考一种粘贴方案,并回答下列问题: