题目内容
7.锂广泛用于电池、贮氢等领域,锂在化合物中显+1价,如图周期表中的信息及4种粒子的结构示意图.
(1)B、C、D、E、F中,D和E(填编号)属于同种元素;
(2)B、C、D、E、F中,C和D(填编号)化学性质相似;
(3)LiMnO2是一种电极材料,其中Mn的化合价为+3;
(4)用化学符号表示:
2个水分子2H2O;2个氦原子2He;2个氦分子2He;
n个铵根离子nNH4+;硝酸根NO3-;2个亚铁离子2Fe2+;
氯化铝AlCl3;氯化钙CaCl2;氢氧化钡Ba(OH)2;硫酸钾K2SO4;
由硅原子和氧原子构成的化合物(该物质中,硅原子和氧原子的个数比为1:2)SiO2.
分析 元素是具有相同核电荷数(即质子数)的一类原子的总称;
化合物中元素化合价代数和为零;
利用元素符号和相应的数字可以表示分子、原子、离子和物质的化学式.
解答 解:(1)B、C、D、E、F中,D和E属于同种元素,这是因为它们的核电荷数相同.
故填:D;E.
(2)B、C、D、E、F中,C和D化学性质相似,这是因为C是氦原子,不容易得失电子,化学性质稳定,D是锂离子,不容易得失电子,化学性质稳定.
故填:C;D.
(3)LiMnO2是一种电极材料,其中锂元素化合价是+1,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,Mn的化合价是+3.
故填:+3.
(4)2个水分子可以表示为2H2O;
2个氦原子可以表示为2He;
2个氦分子可以表示为2He;
n个铵根离子可以表示为nNH4+;
硝酸根可以表示为NO3-;
2个亚铁离子可以表示为2Fe2+;
氯化铝可以表示为AlCl3;
氯化钙可以表示为CaCl2;
氢氧化钡可以表示为Ba(OH)2;
硫酸钾可以表示为K2SO4;
由硅原子和氧原子构成的化合物(该物质中,硅原子和氧原子的个数比为1:2),则该物质是二氧化硅,可以表示为SiO2.
故填:2H2O;2He;2He;nNH4+;NO3-;2Fe2+;AlCl3;CaCl2;Ba(OH)2;K2SO4;SiO2.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
17.一定质量的某化合物完全燃烧,消耗9.6g氧气,生成8.8g二氧化碳和5.4g水.对该化合物的组成判断正确的是( )
| A. | 只含有C、H两种元素 | B. | 含有C、H、O三种元素 | ||
| C. | 分子中C、H原子个数比为3:1 | D. | 以上答案都不正确 |
18.你和小明在实验室中完成二氧化碳气体的性质实验:在试管中加入2ml蒸馏水,滴入2滴石蕊试液,然后通入二氧化碳气体,观察到颜色由紫色变为红色.那么是什么物质使得石蕊试液颜色发生改变呢?
小明提出猜想:①水能使石蕊试液变色;②二氧化碳气体能使石蕊试液变色
设计实验:取用石蕊试液染成的紫色的干燥紫花分别进行如下实验.
从上面的实验可知小明的猜想都不正确,那么你的猜想是二氧化碳和水反应生成的碳酸使石蕊试液变色
实验方案现象结论及原因:
通过以上探究实验可知:往石蕊试液中通入二氧化碳气体,使石蕊试液变色的物质是碳酸.
小明提出猜想:①水能使石蕊试液变色;②二氧化碳气体能使石蕊试液变色
设计实验:取用石蕊试液染成的紫色的干燥紫花分别进行如下实验.
| 实验方案 | 现象 | 结论 | |
| 1 |  往紫花上喷水 | 紫花不变色 | 猜想①不正确 |
| 2 |  把紫花直接放入二氧化碳气体中 | 紫花不变色 | 猜想②不正确 |
| 实验方案 | 现象 | 结论及原因 |
 紫花喷水后放入二氧化碳气体中 | 紫花变红色 | 1、你的猜想正确; 2、使紫花变色的原因是(用文字表达式表示): 二氧化碳+水→碳酸 |
通过以上探究实验可知:往石蕊试液中通入二氧化碳气体,使石蕊试液变色的物质是碳酸.
17.下列化学反应属于复分解反应的是( )
| A. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | B. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | ||
| C. | BaCl2+2AgNO3═2AgCl↓+Ba(NO3)2 | D. | H2CO3═CO2↑+H2O |
 我们生活的世界丰富多彩、变化多端是因为组成世界的物质丰富多样,不断变化所致.
我们生活的世界丰富多彩、变化多端是因为组成世界的物质丰富多样,不断变化所致.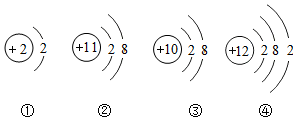 根据下列几种粒子的结构示意图,回答问题.
根据下列几种粒子的结构示意图,回答问题.