题目内容
9.三毛同学家中水龙头锈蚀烂了,去超市新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液…铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
实验 方案 | 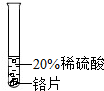 | 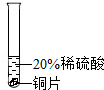 | 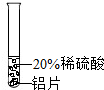 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al Cr Cu | |||
(1)用砂纸打磨金属片的目的是除去金属表面氧化物.
(2)实验三所发生反应的化学方程式是2Al+3H2SO4═Al2(SO4)3+3H2↑.
(3)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是Al、CrSO4溶液、Cu.
【反思归纳】比较金属活动性强弱的方法有:①通过金属与酸反应判断金属活动性强弱;②通过金属与盐溶液反应判断金属活动性强弱.
分析 【实验过程】根据所学金属活动顺序可知铜不能与硫酸反应,铝可以与硫酸反应,进而解决问题.
【考考你】(1)打磨金属表面一般是除去表面的氧化物薄膜;
(2)根据题中信息,书写铝与硫酸的反应方程式进行解答;
(3)用三种药品是最简单的实验方法,可以用Al、CrSO4溶液、Cu;也可以用Al2(SO4)3溶液、Cr、CuSO4溶液;
【反思归纳】可结合实验的过程及课本知识进行总结.
解答 解:根据我们学过的知识可知,铜与稀硫酸不反应,根据图示现象可知,铝与稀硫酸反应比较快.
故答案为:实验现象:无明显现象;结论:铝能与稀硫酸发生反应,反应速率较快;Al Cr Cu;
【考考你】
(1)因为比较活泼的金属表面有一层氧化膜,不活泼的表面有污物.
故答案为:除去金属表面氧化物(或污物)
(2)由资料可知,铝能与稀硫酸反应,生成硫酸铝和氢气,化学方程式:2Al+3H2SO4═Al2(SO4)3+3H2↑
故填:2Al+3H2SO4═Al2(SO4)3+3H2↑;
(3)用三种药品是最简单的实验方法,可以用Al、CrSO4溶液、Cu;也可以用Al2(SO4)3溶液、Cr、CuSO4溶液.
故填:Al、CrSO4溶液、Cu(或Al2(SO4)3溶液、Cr、CuSO4溶液);
【反思归纳】比较金属活动性强弱的方法有:①通过金属与酸反应判断金属活动性强弱;②通过金属与盐溶液反应判断金属活动性强弱.
点评 金属活动顺序表是中考重要考点之一,不但要熟记,还要认真理解并加以运用.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
4. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应为化合反应 | |
| B. | 乙可能为该反应的催化剂 | |
| C. | 反应结束时,甲、丁的质量之比为8:1 | |
| D. | 参加反应的丙、丁质量比为2:3 |
17.下列实验操作正确的是( )
| A. | 为使配制更为准确,在量筒中配制100毫升10%的NaOH溶液 | |
| B. | 为了防止滤液溢出,过滤时滤纸边缘应高于漏斗边缘 | |
| C. | 测定溶液酸碱性时,为使现象更明显,加入的指示剂越多越好 | |
| D. | 检验碳酸盐和酸反应时产生的气体是否为CO2,应将气体通入澄清石灰水 |
14.近年来雾霾频现,大气质量堪忧.下列做法不利于保护大气环境的是( )
| A. | 发展水力、风力发电 | B. | 露天焚烧秸秆、树叶 | ||
| C. | 城市街道洒水降尘 | D. | 乘坐公交车或地铁出行 |
1.在迎接义务教育均衡发展检查的准备工作中,小星同学协助老师将药品分类放入药品柜中,柜中已存放的部分药品如表:
小星应将桌上装有生石灰和活性炭的试剂瓶分别放入药品柜的标号是( )
| 柜卡编号 | ① | ② | ③ | ④ | … |
| 药品 | 硫粉 红磷 | 氧化铜 二氧化锰 | 熟石灰 烧碱 | 氯化钙 硫酸铜 | … |
| A. | ③和① | B. | ④和③ | C. | ②和① | D. | ③和② |
 的微粒符号S2-; 氧化铝中铝元素化合价${\stackrel{+3}{Al}}_{2}$O3.
的微粒符号S2-; 氧化铝中铝元素化合价${\stackrel{+3}{Al}}_{2}$O3.
