题目内容
13.要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是( )| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | O2 | 水蒸气 | 通过浓H2SO4 |
| B | C | CuO | 加入过量的H2SO4溶液,过滤 |
| C | NaCl溶液 | BaCl2 | 加入过量的Na2CO3溶液,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入过量的铁粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、浓硫酸具有吸水性,且不与氧气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、CuO能与过量的稀硫酸反应生成硫酸铜和水,C不与稀硫酸反应,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、BaCl2能与过量的Na2CO3溶液反应生成碳酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质碳酸钠(过量的),不符合除杂原则,故选项所采取的方法错误.
D、过量的铁粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
4.掌握化学用语是学好化学的关键,下列化学用语与所表达的意义相符合的是( )
①FeCl2--氯化亚铁 ②2Ca2+--2个钙离子 ③O2--2个氧原子 ④2H--2个氢元素 ⑤H2O--1个水分子 ⑥$\stackrel{+1}{Na}$--钠离子 ⑦$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
①FeCl2--氯化亚铁 ②2Ca2+--2个钙离子 ③O2--2个氧原子 ④2H--2个氢元素 ⑤H2O--1个水分子 ⑥$\stackrel{+1}{Na}$--钠离子 ⑦$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
| A. | ①④⑤⑦ | B. | ②③④⑥ | C. | ①②⑤⑦ | D. | ②⑤⑥⑦ |
8.下列叙述,你认为科学的是( )
| A. | 洗涤剂去除油污是因为洗涤剂可以溶解油污 | |
| B. | 钢丝球洗刷铝制炊具 | |
| C. | 霉变大米加热后可食用 | |
| D. | 减少使用塑料制品可以减少白色污染 |
5.废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如图所示:

(1)在反应器中发生反应的化学方程式除 Fe2(SO4)3+Fe=3FeSO4外,还有Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)滤液 M 中肯定含有的溶质的离子是Fe2+、H+、SO42-(填离子符号).
(3)在实验室中完成操作 A 的名称是过滤.
(4)滤液 M 经过操作 B 可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
根据溶解度表,硫酸亚铁晶体(FeSO4•7H2O)冷却结晶温度最高不超过60℃.

(1)在反应器中发生反应的化学方程式除 Fe2(SO4)3+Fe=3FeSO4外,还有Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)滤液 M 中肯定含有的溶质的离子是Fe2+、H+、SO42-(填离子符号).
(3)在实验室中完成操作 A 的名称是过滤.
(4)滤液 M 经过操作 B 可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
3.下列物质中碳元素的化合价为+4的是( )
| A. | C | B. | CO | C. | CO2 | D. | CH4 |
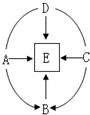 A~E是初中化学常见的物质,它们的相互关系如右图所示(图中“→”代表物质在一定条件下发生转化,“--”表示物质间可以相互反应).其中A和B都属于碳酸盐,且B可用于补钙,C是碱,E是最常用的溶剂.请回答下列问题:
A~E是初中化学常见的物质,它们的相互关系如右图所示(图中“→”代表物质在一定条件下发生转化,“--”表示物质间可以相互反应).其中A和B都属于碳酸盐,且B可用于补钙,C是碱,E是最常用的溶剂.请回答下列问题: