题目内容
12.碳、氧循环是自然界中物质和能量循环的重要组成部分.请根据下图回答下列问题: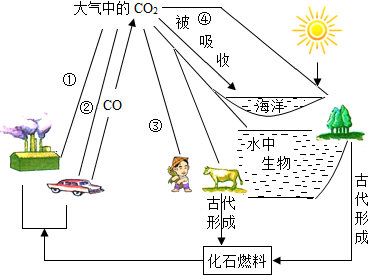
(1)自然界中存在着碳循环,请在图中①-④线上补加箭头(其他箭头已画出),正确表示碳循环中的各种变化关系.
(2)大气中消耗二氧化碳主要途径有植物的光合作用和被海洋吸收.绿色植物在光照作用下可将二氧化碳和水转化生成葡萄糖(C6H12O6)和氧气,其反应的化学方程式为6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿素}$C6Hl206+6O2.
(3)自然界中存在着氧循环,以下为自然界中发生的一些变化:①金属锈蚀②煤炭燃烧③人与动物呼吸④陆地、水生植物的光合作用.从①~④中选择填空,其中消耗氧气的有①②③(填数字序号,下同),产生氧气的有④.
(4)任何物质都具有两面性,我们应趋利避害.如近些年来,化石燃料的过度使用,导致大气中二氧化碳含量增加,进而产生温室效应,但是二氧化碳对人类又是不可缺少的.二氧化碳对地球生命具有的重要意义是没有二氧化碳,光合作用就不会发生,绿色植物就不会存在,人和其他动物也就会失去生存基础;没有二氧化碳,甚至地球也可能变成冰球.
分析 生态系统的碳循环中,碳元素在无机环境与生物群落之间是以二氧化碳的形式通过光合作用进入生物群落,通过生物群落的呼吸作用和含碳有机物及化石燃料的燃烧以二氧化碳的形式返回无机环境,在生物群落内,碳元素以含碳有机物的形式进行流动.在叶绿体中,绿色植物通过光合作用把水和二氧化碳转化为葡萄糖,同时释放出氧气.
解答 解:(1)据图分析,图中的碳循环过程还需要增加①②③指向大气中的二氧化碳,④指向大树等,才能表示碳循环中的各种变化关系,如下图所示:
(2)大气中消耗二氧化碳主要途径有植物的光合作用和被海洋吸收;
在叶绿体中,绿色植物通过光合作用把水和二氧化碳转化为葡萄糖,同时释放出氧气;光合作用的化学方程式为:6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿素}$C6Hl206+6O2.
故填:被海洋吸收;6CO2+6H2O$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{叶绿素}$C6Hl206+6O2.
(3)①金属锈蚀是金属与氧气发生的缓慢氧化,消耗氧气;②化石燃料燃烧需要助燃物氧气,消耗氧气;③人与动物的呼吸是吸入氧气,呼出二氧化碳,消耗氧气;④陆地、水生植物的光合作用是将二氧化碳和水转化成葡萄糖和氧气,释放氧气.
故填:①②③;④.
(4)二氧化碳对地球生命具有的重要意义是:没有二氧化碳,光合作用就不会发生,绿色植物就不会存在,人和其他动物也就会失去生存基础;没有二氧化碳,甚至地球也可能变成冰球.
故填:没有二氧化碳,光合作用就不会发生,绿色植物就不会存在,人和其他动物也就会失去生存基础;没有二氧化碳,甚至地球也可能变成冰球.
点评 二氧化碳的含量较多会引起温室效应,所以我们应大量的植树造林,以减少空气中二氧化碳的含量.

| A. | 干冰升华 | B. | 石墨制成金刚石 | C. | 活性炭吸附异味 | D. | 冰撑破水缸 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 | |
| B. | N2 (O2):将气体缓缓通过灼热的铜 | |
| C. | CaCO3 (CaCl2):加水溶解一过滤一洗涤一干燥 | |
| D. | KCl溶液(K2CO3):加入适量的稀盐酸 |
 用氯气或液氯消毒饮用水时,会和水中的有机物发生反应,生成对人体有毒的有机物.因此,世界环保联盟将全面禁止用氯气对饮用水消毒,建议推广采用安全、高效杀菌消毒剂ClO2.ClO2 是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃.冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于Cl2,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味.
用氯气或液氯消毒饮用水时,会和水中的有机物发生反应,生成对人体有毒的有机物.因此,世界环保联盟将全面禁止用氯气对饮用水消毒,建议推广采用安全、高效杀菌消毒剂ClO2.ClO2 是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃.冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于Cl2,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味. 如图是初中化学中几种常见物质之间的相互转化关系.已知常温下A、B、C为无色气体,且A是一种有毒气体;A、B是由两种相同的元素组成,D、G是由相同的两种元素组成的无色液体;E、F均为黑色固体,且F能与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).
如图是初中化学中几种常见物质之间的相互转化关系.已知常温下A、B、C为无色气体,且A是一种有毒气体;A、B是由两种相同的元素组成,D、G是由相同的两种元素组成的无色液体;E、F均为黑色固体,且F能与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).