题目内容
2.如图各组粒子中前者是A粒子,后者是B粒子的结构示意图中,能形成AB2型化合物一组粒子是( )| A. |  | B. | 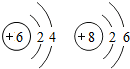 | C. |  | D. |  |
分析 根据原子结构示意图最外层电子的数目与元素形成化物所显示的化合价的关系,推断形成化合物的化学式.离子所带正负电荷数与化合价数值的关系:数值与正负都相同,只是书写位置不同,数字与正负号前后顺序不同.
解答 解:A、两元素的核电荷数为12和8,可知A、B两元素分别为Mg、O,它们能形成一种化合物MgO,不可以形成AB2型化合物,故不符合题意.
B、两元素的核电荷数为6和8,可知A、B两元素分别为C、O,它们能形成CO2、CO两种化合物,可以形成AB2型化合物,故符合题意.
C、两元素的核电荷数为2和17,则可推知A、B两元素分别为He和Cl,He不活泼,难形成化合物,故不符合题意.
D、两元素的核电荷数为11和8,则可推知A、B两元素分别为Na和O,可形成Na2O,不能形成AB2型化合物
,故不符合题意.
故选B.
点评 本题考查根据原子的结构示意图和元素化合价的关系书写化学式,考查知识点较多,既考查了对原子结构的理解,又考查了元素化合价的确定和化学式的书写,题目难度稍大,易出错.

练习册系列答案
相关题目
10.“酒香不怕巷子深”这是因为( )
| A. | 分子之间有间隔 | |
| B. | 分子的质量和体积都很小 | |
| C. | 分子是保持物质化学性质的最小粒子 | |
| D. | 分子在不断地运动 |
17.研究学习小组选择“活性炭的吸附效果和哪些因素有关”的课题进行研究,以下是他们探究的过程:
提出假设:活性炭的吸附效果和活性炭的量有关
完成实验:按下表进行实验,取容积相同的集气瓶(125mL),收集满红棕色的二氧化氮气体,并进行编号,记录颜色消失的时间.
分析数据,得出结论
要完成本实验,实验标号2中活性炭的纯度应该为80%
(1)该探究过程得出的结论是:相同条件下,活性炭量越多,吸附效果越好
(2)反思:(1)某品牌冰箱的除味剂主要成分是活性炭,其说明书中写到“切勿靠近高温”,原因是活性炭具有(用化学方程式表示):C+O2$\frac{\underline{\;高温\;}}{\;}$CO2
(2)活性炭的吸附效果还和那些因素有关?请你帮他们继续探究(只要求提出假设和实验方案).
假设:活性炭的吸附效果和表面积有关
实验方案:取相同质量的活性炭两份,1份颗粒较大,1份颗粒较小,分别放入容积相同的收集满红棕色的二氧化氮气体的集气瓶中,观察红棕色消失的时间.
提出假设:活性炭的吸附效果和活性炭的量有关
完成实验:按下表进行实验,取容积相同的集气瓶(125mL),收集满红棕色的二氧化氮气体,并进行编号,记录颜色消失的时间.
| 实验编号 | 活性炭纯度 | 活性炭的用量(克) | 消失时间(秒) |
| 1 | 80% | 1.0 | 60 |
| 2 | 9.0 | 45 |
要完成本实验,实验标号2中活性炭的纯度应该为80%
(1)该探究过程得出的结论是:相同条件下,活性炭量越多,吸附效果越好
(2)反思:(1)某品牌冰箱的除味剂主要成分是活性炭,其说明书中写到“切勿靠近高温”,原因是活性炭具有(用化学方程式表示):C+O2$\frac{\underline{\;高温\;}}{\;}$CO2
(2)活性炭的吸附效果还和那些因素有关?请你帮他们继续探究(只要求提出假设和实验方案).
假设:活性炭的吸附效果和表面积有关
实验方案:取相同质量的活性炭两份,1份颗粒较大,1份颗粒较小,分别放入容积相同的收集满红棕色的二氧化氮气体的集气瓶中,观察红棕色消失的时间.
18.鉴别一杯硝酸钾溶液是否饱和的方法是( )
| A. | 加热 | B. | 降温 | ||
| C. | 加硝酸钾固体 | D. | 加该温度下的硝酸钾饱和溶液 |
 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线.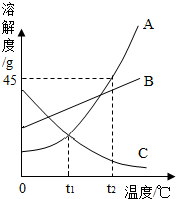 如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题: