题目内容
13.在AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中,加入过量的铁粉,充分反应后过滤,滤液中大量存在的金属离子是( )| A. | 只有Ag+ | B. | 只有Fe2+ | C. | Ag+和Cu2+ | D. | Zn2+和Fe2+ |
分析 在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:在金属活动性顺序中,锌>铁>铜>银,将过量的铁粉放入含AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液里,铁能与硝酸银发生置换反应生成银和硝酸亚铁,能与硝酸铜反应生成硝酸亚铁和铜,由于铁过量,AgNO3和Cu(NO3)2全反应;不能与硝酸锌发生置换反应,故溶液中含有锌离子和亚铁离子;
故选D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
8.将6000L氧气在加压下,可装入容积为40L的钢瓶内,这一事实证明( )
| A. | 分子在不断运动 | B. | 分子间有间隔 | C. | 分子的体积很小 | D. | 分子的质量很小 |
18.微观示意图有助于我们认识化学物质和理解化学反应.甲是一种比较清洁的燃料,已知甲和乙能在一定条件下反应生成丙和丁.
(1)甲、乙、丙、丁中属于单质的是乙(填序号,下同),属于氧化物的是丙、丁.
(2)该反应中,乙和丁的质量比为12:11.
| 物 质 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 | 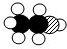 |  | 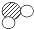 |  |
(2)该反应中,乙和丁的质量比为12:11.
5.研究发现,元素原子如果最外层电子数是4,其单质在导电方面具有某些特殊的优良性能,如硅原子最外电子层电子数为4,常用作半导体材料.下列可作半导体材料的是( )
| A. | 铝 Al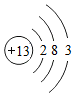 | B. | 氧 O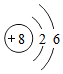 | C. | 锗 Ge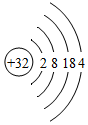 | D. | 氖 Ne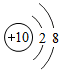 |
2.根据下列三个化学方程式:①Z+Y$\frac{\underline{\;高温\;}}{\;}$2X②2X+O2$\frac{\underline{\;点燃\;}}{\;}$2Z③2CuO+Y$\frac{\underline{\;高温\;}}{\;}$2Cu+Z,试确定X、Y、Z的一组物质是( )
| A. | C、CO、CO4 | B. | CO、CO3、C | C. | C、CO2、CO | D. | CO、C、CO2 |
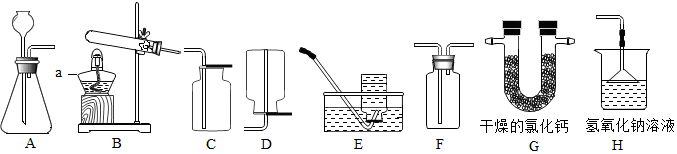
3.正确的操作能保证化学实验的顺利进行.下列实验操作不正确的是( )
| A. | 氢氧化钠固体要放在纸上称量 | |
| B. | 点燃一氧化碳气体前,应先检验气体的纯度 | |
| C. | 为了节约药品,实验室用剩的药品应放回原瓶 | |
| D. | 用量筒量取一定量的液体时,仰视或俯视读数 | |
| E. | 测定溶液的pH时,将试纸直接放入待测液中 | |
| F. | 配制稀硫酸时,将浓硫酸沿烧杯壁慢慢加入水中,并不断搅拌 | |
| G. | 用高锰酸钾制取所需氧气后,先把导管从水槽中移除再将酒精灯熄灭 |
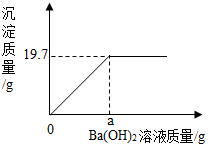 固体氢氧化钠放置在空气中容易变质转化为碳酸钠,现称取一久置于空气中的烧碱样品10.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示,请通过计算回答:
固体氢氧化钠放置在空气中容易变质转化为碳酸钠,现称取一久置于空气中的烧碱样品10.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示,请通过计算回答: