题目内容
17.结合下列实验装置图回答问题: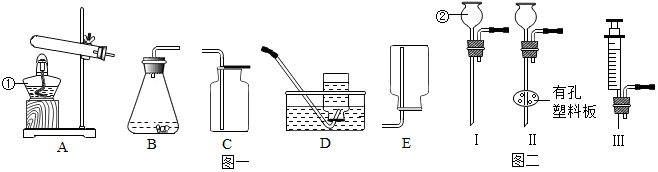
(1)写出图中带标号仪器的名称:①锥形瓶②长颈漏斗.
(2)请从图一中选择合适的装置在实验室中制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
检验该气体的方法是将带火星木条伸入集气瓶中,看是否复燃;选择的发生装置是A(填序号,下同),选择的收集装置是C或D,选择此收集装置的理由是氧气的密度大于空气的密度,并且不易溶于水.
(3)装置B虽然操作简便,但无法控制反应速率.请从图二中选取Ⅲ(填序号)取代B中的单孔塞,以达到控制反应速率的目的.
分析 (1)根据常见仪器的名称、用途进行分析.
(2)根据用高锰酸钾制取氧气的反应物、反应条件、生成物写出化学方程式;根据氧气能支持燃烧确定检验氧气的方法即可;根据反应物的状态和反应条件选择发生装置;根据氧气的密度和溶水性选择收集装置.
(3)固液常温型装置制取气体控制反应速度时可以通过控制液体滴加速度.
解答 解:(1)图中①是锥形瓶,②是长颈漏斗.
故答案为:锥形瓶;长颈漏斗.
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰、氧气,化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;由于氧气能支持燃烧,故检验氧气的方法可将带火星木条伸入集气瓶中,看是否复燃;因是固体的加热反应,所以选择A作为发生装置;氧气的密度大于空气的密度,并且不易溶于水,所以可以用向上排空气法和排水法收集.
故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;将带火星木条伸入集气瓶中,看是否复燃;A;C或D;氧气的密度大于空气的密度,且不易溶于水.
(3)Ⅰ只能随时添加液体,不能控制反应速率,Ⅱ只能使反应随开随停,不能控制反应速率,Ⅲ可以控制稀盐酸的滴加速度从而控制反应速率.
故答案为:Ⅲ.
点评 此题考查的是气体的制取原理和装置的选择.只要掌握气体的制取原理,掌握装置选择的依据,问题就能迎刃而解.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
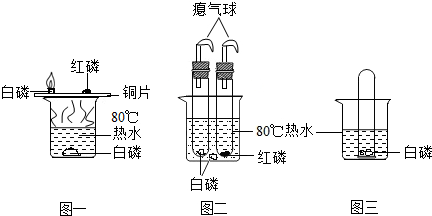
8.某兴趣小组活动中,同学们 按图11装置对“可燃物燃烧的条件”进行探究.探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问.
[查阅资料]白磷的着火点是40℃,红磷 的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
[交流与讨论]白烟对人体健康有害,该实验装置必须改进.
[改进与实验]同学们按改进后的图12装置进行实验,请你帮助他们将下表补充完整.
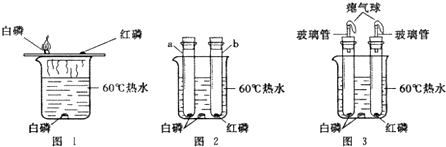
[反思与评价](1)改进后的图2装置与图1装置比较,优点是防止白磷燃烧产生的五氧化二磷扩散,污染环境和危害人体健康.
(2)小林指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是避免橡皮塞因试管内气体热膨胀飞出,造成安全事故.
[拓展与迁移]实验小结时,小朱说:“待a试管冷却后,如将试管口紧贴水面(室温下).并取下橡皮塞,将看到液体进入试管”.这一说法得到大家的一致认同.小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测.甲:接近试管容积的$\frac{1}{5}$;乙:不一定接近试管容积的$\frac{1}{5}$.
你赞同的预测是乙 (填“甲”或“乙”),理由是白磷的量不清楚,所以无法确定是否能够完全消耗氧气.
[查阅资料]白磷的着火点是40℃,红磷 的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
[交流与讨论]白烟对人体健康有害,该实验装置必须改进.
[改进与实验]同学们按改进后的图12装置进行实验,请你帮助他们将下表补充完整.

| 现象 | 解释 |
| 试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. | b试管中红磷、热水中白磷都没有燃烧的原因是①温度未达到红磷的着火点,②热水中的白磷没有与氧气(或空气)接触. |
(2)小林指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是避免橡皮塞因试管内气体热膨胀飞出,造成安全事故.
[拓展与迁移]实验小结时,小朱说:“待a试管冷却后,如将试管口紧贴水面(室温下).并取下橡皮塞,将看到液体进入试管”.这一说法得到大家的一致认同.小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测.甲:接近试管容积的$\frac{1}{5}$;乙:不一定接近试管容积的$\frac{1}{5}$.
你赞同的预测是乙 (填“甲”或“乙”),理由是白磷的量不清楚,所以无法确定是否能够完全消耗氧气.
12.在刚过去的2010年里,包括四川在内的我国西南地区遭遇历史罕见的特大旱灾,造成数以十万计的人畜饮水困难.这次的自然灾害又一次让我们增强了节约用水的意识.下列做法与节约用水无关的是( )
| A. | 用喷灌、滴灌方法给农作物浇水 | |
| B. | 加大力度开发利用地下水 | |
| C. | 关停一些污染大、用水量大、产能低的工厂 | |
| D. | 洗衣、洗菜、淘米水用来浇花、拖地、冲厕所 |
6.下列各种现象,都属于化学变化的一组是( )
| A. | 食物腐烂、钢铁生锈 | B. | 汽油挥发、木炭燃烧 | ||
| C. | 水分蒸发、滴水成冰 | D. | 蜡烛熔化、白磷自燃 |