题目内容
 用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品5.5g,充分溶解于44g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求:
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品5.5g,充分溶解于44g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求:(1)该纯碱样品中碳酸钠的质量分数.(精确到0.1%)
(2)所加入氯化钙溶液的溶质质量分数.
(3)求恰好完全反应时溶液中溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)计算该纯碱样品中碳酸钠的质量分数,先根据化学方程式求出样品中碳酸钠的质量,再利用质量分数公式计算即可.
(2)计算所加入氯化钙溶液的溶质质量分数,先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
(3)计算恰好完全反应时溶液(氯化钠溶液)中溶质质量分数,先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
(2)计算所加入氯化钙溶液的溶质质量分数,先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
(3)计算恰好完全反应时溶液(氯化钠溶液)中溶质质量分数,先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
解答:解:设该纯碱样品中碳酸钠的质量为x,55.5g氯化钙溶液中溶质的质量为y,生成的氯化钠的质量为z,
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100 117
x y 5.0g z
(1)
=
x=5.3g
该纯碱样品中碳酸钠的质量分数为
×100%≈96.4%.
(2)
=
y=5.55g
所加入氯化钙溶液的溶质质量分数为
×100%=10%.
(3)
=
z=5.85g
恰好完全反应时溶液中溶质质量分数为
×100%=6.05%.
答:(1)该纯碱样品中碳酸钠的质量分数为96.4%;(2)所加入氯化钙溶液的溶质质量分数为10%;(3)恰好完全反应时溶液中溶质质量分数为6.05%.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100 117
x y 5.0g z
(1)
| 106 |
| 100 |
| x |
| 5.0g |
该纯碱样品中碳酸钠的质量分数为
| 5.3g |
| 5.5g |
(2)
| 111 |
| 100 |
| y |
| 5.0g |
所加入氯化钙溶液的溶质质量分数为
| 5.55g |
| 55.5g |
(3)
| 100 |
| 117 |
| 5.0g |
| z |
恰好完全反应时溶液中溶质质量分数为
| 5.85g+5.5g-5.3g |
| 5.5g+44g+55.5g-5.0g |
答:(1)该纯碱样品中碳酸钠的质量分数为96.4%;(2)所加入氯化钙溶液的溶质质量分数为10%;(3)恰好完全反应时溶液中溶质质量分数为6.05%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意题意、图表信息等各种信息,根据图象确定沉淀的质量是正确解答本题的前提和关键.

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
下列物质按酸、碱、盐、混合物顺序排列的是( )
| A、苛性钠、盐酸、食盐、酒精 |
| B、硝酸、熟石灰、小苏打、合金 |
| C、苏打、火碱、硫酸、澄清石灰水 |
| D、醋酸、纯碱、碳酸钙、稀有气体 |
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子
”表示氧原子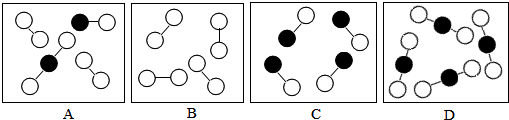
 现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.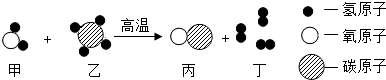

 A、B、C、D是初中化学中常见的物质,其中A、B都由两种相同元素组成,C、D均为气体单质,人和动物吸入C 后,体内的营养物质会发生缓慢氧化,它们的转化关系如图所示(反应条件已略去).
A、B、C、D是初中化学中常见的物质,其中A、B都由两种相同元素组成,C、D均为气体单质,人和动物吸入C 后,体内的营养物质会发生缓慢氧化,它们的转化关系如图所示(反应条件已略去). ”表示碳原子,“
”表示碳原子,“ ”表示氧原子.
”表示氧原子.