题目内容
10.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能只是CaCl2
(C)溶质可能是CaCl2与盐酸
【实验探究】
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色
酚酞试液.振荡.观察到酚酞试液不变色.于是他排除了猜想(A),你认为他排除猜想(A)的理由是氢氧化钙溶液呈碱性,能使酚酞试液变红.
通过实验探究,最后确定猜想(C)正确.
【反思与拓展】要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量碳酸钙充分反应后过滤,反应的方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 根据题中的叙述找出反应物、生成物,根据方程式的书写规则进行书写方程式,氢氧化钙和盐酸反应生成了氯化钙和水;酚酞遇碱性溶液变红,遇中性或是酸性溶液不变色,可以据此解答;要得到氯化钙溶液,就是除去盐酸,根据盐酸能与碳酸钙反应解答即可.
解答 解:(1)氢氧化钙和盐酸发生中和反应生成氯化钙和水,故该反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;
(2)①酚酞遇碱性溶液变红,遇中性或是酸性溶液不变色,所以可以判断在反应的溶液中没有氢氧化钙,故填:氢氧化钙溶液呈碱性,能使酚酞试液变红;
【反思与拓展】要得到氯化钙溶液,就是除去盐酸,根据盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳,而过量的碳酸钙对于氯化钙没有影响,可以通过过滤除去,故填:碳酸钙,CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题考查了氢氧化钙的溶解性及与盐酸发生中和反应的程度探究,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
20.如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
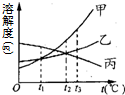

| A. | 在t1℃时,溶解度甲=乙<丙 | |
| B. | 从乙饱和溶液中析出较多量的晶体通常可采用降温结晶法 | |
| C. | 等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙 | |
| D. | t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液的溶质质量分数增大,丙溶液的溶质质量分数减小 |
18.下列说法正确的是( )
| A. | 煤气泄漏,用明火查看 | B. | 明矾净水,能杀菌消毒 | ||
| C. | 油锅着火,可加水浇灭 | D. | 金属回收,可节能防污 |