题目内容
11. 归纳总结是化学息息的常见方法,请根据所学知识回答问题:
归纳总结是化学息息的常见方法,请根据所学知识回答问题:(1)甲+HCl→NaCl+H2O,甲物质可以是NaOH(填化学式).上述转化的化学方程式是NaOH+HCl═NaCl+H2O.
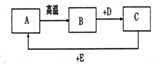
(2)A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).则A为CaCO3(填化学式),写出C→A反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
分析 (1)根据酸和碱反应能生成盐和水进行分析;
(2)根据A、B、C、D、E都是初中化学常见的物质,B、D、E均为氧化物,常温下B为固态,D为液态,E为气态,A、B、C中均含有同一种金属元素,A高温生成的B和D会生成C,所以A是碳酸钙,碳酸钙高温生成氧化钙和二氧化碳,所以B是氧化钙,氧化钙和水反应生成氢氧化钙,所以D是水,C是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以E是二氧化碳,然后将推出的物质进行验证即可.
解答 解:(1)盐酸和氢氧化钠反应生成氯化钠和水,所以甲物质可以是NaOH,化学方程式是:NaOH+HCl═NaCl+H2O;
(2)A、B、C、D、E都是初中化学常见的物质,B、D、E均为氧化物,常温下B为固态,D为液态,E为气态,A、B、C中均含有同一种金属元素,A高温生成的B和D会生成C,所以A是碳酸钙,碳酸钙高温生成氧化钙和二氧化碳,所以B是氧化钙,氧化钙和水反应生成氢氧化钙,所以D是水,C是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以E是二氧化碳,经过验证,推导正确,所以A为CaCO3,C→A得反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故答案为:(1)NaOH,NaOH+HCl═NaCl+H2O;
(2)CaCO3,Ca(OH)2+CO2═CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.向一定质量的FeSO4和CuSO4的混合溶液中加入一定质量的锌粉,充分反应后过滤,得滤液和滤渣,向滤渣中加入稀盐酸,有气泡产生,根据实验现象分析判断下列说法中不正确的是( )
| A. | 滤液的颜色呈蓝色 | B. | 滤液中可能存在Fe2+ | ||
| C. | 滤渣中一定含有Fe、Cu、Zn | D. | 滤渣中一定含有Fe和Cu可能含有Zn |
2.请根据下表回答有关问题:(均用序号填空)
(1)表中的物质属于氧化物的是②;属于碱的是③;属于盐的是④.
(2)若要测定纯碱溶液的酸碱度,选用下列选项中③.
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(3)槟榔芋皮上含有一种碱性的物质--皂角素,沾上它会使皮肤奇痒难忍.你认为可选用下列①来涂抹止痒.
①食醋(含醋酸) ②熟石灰 ③纯碱.
| 序 号 | ① | ② | ③ | ④ |
| 物 质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
(2)若要测定纯碱溶液的酸碱度,选用下列选项中③.
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(3)槟榔芋皮上含有一种碱性的物质--皂角素,沾上它会使皮肤奇痒难忍.你认为可选用下列①来涂抹止痒.
①食醋(含醋酸) ②熟石灰 ③纯碱.
20.煤、石油和天然气被称为三大化石燃料,航空煤油是从石油中提炼出来的.C919发动机上的压气机将高密度空气压入燃烧室,促进了航空煤油的燃烧.高密度空气能使航空煤油燃烧更充分的原因是提供了充足的氧气.
17.对下列实验操作和现象的分析合理的是( )
| A. | 通过闻气味区别厨房中的醋和白酒 | |
| B. | 往溶液中滴加氯化钡溶液有白色沉淀,该沉淀一定是BaSO4 | |
| C. | 加入足量稀盐酸可以除去硫酸镁溶液中混有少量的氧化镁 | |
| D. | 降温某溶液有晶体析出,该原溶液一定是饱和溶液 |

 请根据图中的信息回答问题.
请根据图中的信息回答问题.