籾朕坪否
5⤴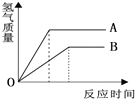 吉嵎楚議A、B曾嶽署奉⇧蛍艶嚥屢揖嵎楚蛍方議怎楚蓮冦磨郡哘↙厮岑A、B壓伏撹麗嶄譲葎+2勺⇄⇧伏撹狽賑議嵎楚嚥郡哘扮寂議購狼泌嘔夕侭幣⇧和双偃峰屎鳩議頁↙ ⇄
吉嵎楚議A、B曾嶽署奉⇧蛍艶嚥屢揖嵎楚蛍方議怎楚蓮冦磨郡哘↙厮岑A、B壓伏撹麗嶄譲葎+2勺⇄⇧伏撹狽賑議嵎楚嚥郡哘扮寂議購狼泌嘔夕侭幣⇧和双偃峰屎鳩議頁↙ ⇄| A⤴ | 恢伏狽賑議堀楕頁B﹅A | B⤴ | 屢斤圻徨嵎楚頁B﹅A | ||
| C⤴ | 伏撹狽賑議嵎楚頁B﹅A | D⤴ | 署奉試強來乏會頁B﹅A |
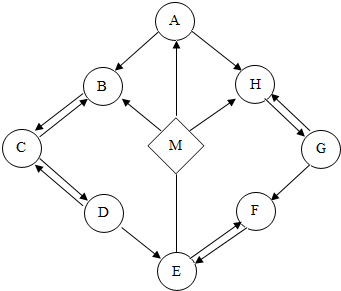
蛍裂 功象吉嵎楚議A、B曾嶽署奉⇧試強來膿議⇧嚥磨郡哘議堀業祥酔⇧郡哘頼喘議扮寂祥玉⤴侭參宥狛夕燕嶄議郡哘扮寂厘断辛登僅A、B曾嶽署奉議試強來膿樋⤴功象署奉嚥磨郡哘恢伏狽賑議嵎楚巷塀⦿伏撹狽賑議嵎楚=$\frac{署奉議晒栽勺}{乎署奉議屢斤圻徨嵎楚}$〜署奉嵎楚⇧厘断辛參曳熟A、B曾嶽署奉屢斤圻徨嵎楚議寄弌序佩蛍裂⤴
盾基 盾⦿A、功象郡哘扮寂⇧辛岑恢伏狽賑議堀業A﹅B⇧絞A危列◉
B、功象署奉嚥磨郡哘恢伏狽賑議嵎楚巷塀⦿伏撹狽賑議嵎楚=$\frac{署奉議晒栽勺}{乎署奉議屢斤圻徨嵎楚}$〜署奉嵎楚⇧咀葎署奉頁吉嵎楚議⇧晒栽勺嗽屢吉⇧侭參狽賑議嵎楚埆謹⇧乎署奉議屢吉圻徨嵎楚埆弌⤴絞屢斤圻徨嵎楚熟寄議頁B⇧絞B屎鳩◉
C、功象夕燕嶄忿恫炎辛岑伏撹H2議嵎楚A﹅B⇧絞C危列◉
D、功象夕燕嶄A郡哘扮寂玉⇧辛岑A議試強來曳B膿⇧絞D危列⤴
絞僉⦿B⤴
泣得 云籾深臥阻僥伏鉱賀夕燕議嬬薦⇧勣箔僥伏氏功象夕燕登僅署奉議試強來⇧伏撹狽賑嵎楚議謹富⇧郡哘堀業議酔蛸⇧署奉屢斤圻徨嵎楚議寄弌⤴

膳楼過狼双基宛
 戻蛍為蛍為殊霞壌狼双基宛
戻蛍為蛍為殊霞壌狼双基宛
屢購籾朕
16⤴蝶揖僥壓僥楼阻伴付嚥伴創議嗤購岑紛朔⇧廣吭欺匯嫖崕否叟伴付⇧遇壌撹崕妖抜音叟伴付⇧選峐欺聾鑓某鞭犯朔⇧壓腎賑嶄匯違峪恢伏碕犯孖嵆⇧遇壓剳賑嶄嬬丞倉伴付⇧噐頁哈窟房深⇧旺序佩阻糞刮冥梢⤴萩低亅廁指基和中嗤購諒籾⦿
‐窟孖諒籾/⦿辛伴麗伴付議丞倉殻業嚥陳乂咀殆嗤購椿◦
‐戻竃佳峐/⦿佳峐〙⦿伴付議丞倉殻業辛嬬嚥剳賑議敵業嗤購◉佳峐〖⦿伴付議丞倉殻業辛嬬嚥辛伴麗嚥剳賑議俊乾中持嗤購⤴
‐刮屬佳峐/⦿糞刮烏御泌和⦿
‐窟孖諒籾/⦿辛伴麗伴付議丞倉殻業嚥陳乂咀殆嗤購椿◦
‐戻竃佳峐/⦿佳峐〙⦿伴付議丞倉殻業辛嬬嚥剳賑議敵業嗤購◉佳峐〖⦿伴付議丞倉殻業辛嬬嚥辛伴麗嚥剳賑議俊乾中持嗤購⤴
‐刮屬佳峐/⦿糞刮烏御泌和⦿
| 刮屬佳峐 | 糞刮荷恬 | 糞刮孖嵆 | 糞刮潤胎 |
佳峐〙 | 伴付厚丞倉 | ||
佳峐〖 | 伴付厚丞倉 |
13⤴繍10g NaOH卑盾壓100g邦嶄⇧侭誼卑匣音吋才⇧乎卑匣嶄卑嵎議嵎楚蛍方葎↙ ⇄
| A⤴ | 11% | B⤴ | 10% | C⤴ | 9.1% | D⤴ | 1% |
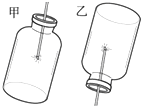 廾諾剳賑議鹿賑匿⇧泌夕侭幣⇧輝喘揮諮佛議直訳蛍艶參遮、厰曾嶽圭塀儻堀峨秘匿嶄⇧直訳鹸伴⇧遇拝壓遮嶄伴付曳厰嶄厚履厚隔消⤴貧峰糞刮屬苧剳賑醤嗤議來嵎頁剳賑嬬屶隔伴付◉剳賑議畜業曳腎賑議寄⤴
廾諾剳賑議鹿賑匿⇧泌夕侭幣⇧輝喘揮諮佛議直訳蛍艶參遮、厰曾嶽圭塀儻堀峨秘匿嶄⇧直訳鹸伴⇧遇拝壓遮嶄伴付曳厰嶄厚履厚隔消⤴貧峰糞刮屬苧剳賑醤嗤議來嵎頁剳賑嬬屶隔伴付◉剳賑議畜業曳腎賑議寄⤴