题目内容
5.某同学在探究铝丝和稀盐酸反应的快慢和什么因素有关系,他设计了三组实验有关的数据如下表,分析之后回答问题.(1)写出铝丝和稀盐酸反应的方程式2Al+6HCl═2AlCl3+3H2↑
| 实验编号 | 稀盐酸中溶质的质量分数 | 反应温度 | 铝丝反应完所需的时间 |
| (1) | 5% | 20°C | 400秒 |
| (2) | 10% | 20°C | 300秒 |
| (3) | 10% | 30°C | 80秒 |
(3)能表明稀盐酸的浓度对反应快慢有影响的实验编号是(1)(2)
(4)若将实验(1)中稀盐酸中溶质的质量分数变成7%,请你推测铝丝反应完的时间的取值范围是300秒~400秒
(5)该实验除了用铝丝反应完的时间来衡量反应速率的快慢,你还能提出别的方法来衡量反应速率的快慢吗?可以根据产生气泡的速率来衡量,产生气泡的速率越快,反应速率越快.
分析 铝和稀盐酸反应生成氯化铝和氢气;
根据表中提供的数据可以判断相关方面的问题;
铝和稀盐酸的反应速率越快,产生的气泡就越快、越多.
解答 解:(1)铝和稀盐酸反应的化学方程式为:2Al+6HCl═2AlCl3+3H2↑.
故填:2Al+6HCl═2AlCl3+3H2↑.
(2)实验(2)和实验(3)中,稀盐酸的浓度相同,30℃比20℃反应需要的时间短,说明30℃比20℃反应的速率快,即该反应速率的快慢和温度有关系.
故填:温度.
(3)能表明稀盐酸的浓度对反应快慢有影响的实验编号是(1)(2),(1)和(2)中,温度相同,稀盐酸的浓度不同,反应需要的时间不同,说明稀盐酸的浓度对反应快慢有影响.
故填:(1)(2).
(4)若将实验(1)中稀盐酸中溶质的质量分数变成7%,则铝丝反应完的时间应该是大于300秒,小于400秒.
故填:300秒~400秒.
(5)因为铝和稀盐酸反应速率越快,产生的气泡就越多、越快,因此可以用产生气泡的速率来衡量反应的快慢.
故填:可以根据产生气泡的速率来衡量,产生气泡的速率越快,反应速率越快.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.现有CO2和CO的混合物30g,测得其中氧元素的质量分数为60%,将混合物通过足量的炙热氧化铜充分反应后,在通入足量的烧碱溶液中,让其充分反应,则生成碳酸钠的质量为 ( )
| A. | 100g | B. | 106g | C. | 96g | D. | 53g |
20.正确的操作是实验成功的关键之一,以下操作正确的是( )
| A. | 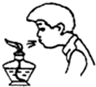 熄灭酒精灯 | B. |  闻气味 | ||
| C. | 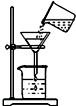 过滤 | D. | 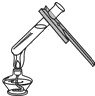 给试管里的液体加热 |
10.A、B、C三种物质各15g,它们化合时只能生成30g新物质D.若增加10g A 则反应停止后,原反应物中只余C.根据上述条件推断下列说法中正确的是( )
| A. | 第一次反应停止后,B剩余9 g | B. | 第二次反应后,D的质量为30 g | ||
| C. | 反应中A和B的质量比是3:2 | D. | 反应中A和C的质量比是5:2 |
14.鉴别O2、CO、CO2三种气体,可行简便的方法是( )
| A. | 将气体分别通入澄清石灰水 | |
| B. | 将气体分别通入石蕊试液 | |
| C. | 试验三种气体在水中溶解性 | |
| D. | 用燃着的木条分别伸入盛有三种气体的试剂瓶内 |
 氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:
氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答: 如图中A烧杯盛有浓氨水,B烧杯内是滴加了几滴酚酞溶液的蒸馏水.过一会儿,观察到的现象是酚酞溶液变红,本实验能说明分子不断运动(答出一条即可).
如图中A烧杯盛有浓氨水,B烧杯内是滴加了几滴酚酞溶液的蒸馏水.过一会儿,观察到的现象是酚酞溶液变红,本实验能说明分子不断运动(答出一条即可). 我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析:
我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析: