题目内容
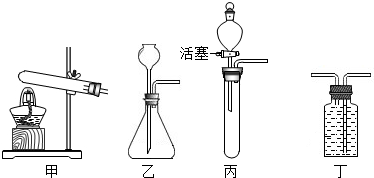 某化学实验小组的同学用如图所示装置进行制备气体的探究.
某化学实验小组的同学用如图所示装置进行制备气体的探究.(1)实验室制取二氧化碳的化学方程式为
(2)通常,在实验室不用碳酸钠和稀盐酸反应来制取CO2.但用丙装置却可以顺利制得.与乙装置相比较,丙装置的显著优点是
(3)现要现要配制100g溶质质量分数为6%的双氧水溶液与二氧化锰来制取氧气,需要30%的过氧化氢溶液溶液
考点:常用气体的发生装置和收集装置与选取方法,混合物的分离方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能使澄清石灰水变浑浊;
显酸性的溶液能使石蕊试液变红色;
(2)不同的实验装置,功能不同;
通常情况下,锌和稀硫酸反应能生成硫酸锌和氢气;
(3)溶液稀释前后,溶质质量不变.
二氧化碳能使澄清石灰水变浑浊;
显酸性的溶液能使石蕊试液变红色;
(2)不同的实验装置,功能不同;
通常情况下,锌和稀硫酸反应能生成硫酸锌和氢气;
(3)溶液稀释前后,溶质质量不变.
解答:解:(1)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCL═CaCL2+CO2↑+H2O;
该操作不能达到检验二氧化碳的目的,是因为盐酸具有挥发性,挥发出的氯化氢气体也能使石蕊试液变红.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;不能;盐酸具有挥发性,挥发出的氯化氢气体也能使石蕊试液变红.
(2)与乙装置相比较,丙装置的显著优点是可以控制反应速率;
锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
若用丁装置收集气体应从左端进入.
故填:能够控制反应速率;Zn+H2SO4═ZnSO4+H2↑;左.
(3)设需要30%的过氧化氢溶液质量为x,
x×30%=100g×6%,
x=20g,
其中二氧化锰起催化作用,从反应后的溶液中回收二氧化锰的主要操作步骤是溶解、过滤、蒸发.
故填:20;催化;溶解、过滤、蒸发.
该操作不能达到检验二氧化碳的目的,是因为盐酸具有挥发性,挥发出的氯化氢气体也能使石蕊试液变红.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;不能;盐酸具有挥发性,挥发出的氯化氢气体也能使石蕊试液变红.
(2)与乙装置相比较,丙装置的显著优点是可以控制反应速率;
锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
若用丁装置收集气体应从左端进入.
故填:能够控制反应速率;Zn+H2SO4═ZnSO4+H2↑;左.
(3)设需要30%的过氧化氢溶液质量为x,
x×30%=100g×6%,
x=20g,
其中二氧化锰起催化作用,从反应后的溶液中回收二氧化锰的主要操作步骤是溶解、过滤、蒸发.
故填:20;催化;溶解、过滤、蒸发.
点评:本题考查仪器的用途、装置的选择、化学方程式的书写、实验基本操作等方面的知识,只有综合掌握教材内容才能正确的做出解答.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
下列对生产、生活现象的解释正确的是( )
| A、温度计里的汞柱下降是因为原子随温度的降低而变小 |
| B、在花园里可嗅到花香是因为分子在不断运动 |
| C、玻璃破碎无法复原是因为分子间存在斥力 |
| D、铝锭难被压缩是因为铝原子间没有间隙 |



 兴趣小组的同学研究(Cu-Zn合金)样品中锌的含量,取该样品18g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如图所示.请计算:
兴趣小组的同学研究(Cu-Zn合金)样品中锌的含量,取该样品18g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如图所示.请计算: