题目内容
 兴趣小组的同学研究(Cu-Zn合金)样品中锌的含量,取该样品18g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如图所示.请计算:
兴趣小组的同学研究(Cu-Zn合金)样品中锌的含量,取该样品18g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如图所示.请计算:(1)18g该样品中锌的质量.
(2)稀硫酸中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:Cu-Zn合金中锌的活动性比氢强,能与稀硫酸反应,铜不能;由产生氢气的质量与所用稀硫酸的质量关系图可知,该样品18g跟足量的稀硫酸充分反应,产生氢气的质量为0.2g,恰好完全反应消耗的稀硫酸的质量为100g,据此由锌和稀硫酸反应的化学方程式,进行分析解答.
解答:解:该样品18g跟足量的稀硫酸充分反应,产生氢气的质量为0.2g.
设18g该样品中锌的质量为x,稀硫酸中溶质的质量为y,
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.2g
=
x=6.5g
=
y=9.8g
稀硫酸中溶质的质量分数为
×100%=9.8%.
答:(1)18g该样品中锌的质量为6.5g;(2)稀硫酸中溶质的质量分数为9.8%.
设18g该样品中锌的质量为x,稀硫酸中溶质的质量为y,
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.2g
| 65 |
| 2 |
| x |
| 0.2g |
| 98 |
| 2 |
| y |
| 0.2g |
稀硫酸中溶质的质量分数为
| 9.8g |
| 100g |
答:(1)18g该样品中锌的质量为6.5g;(2)稀硫酸中溶质的质量分数为9.8%.
点评:本题难度较大,主要考查学生根据图表数据、化学方程式的计算进行解决问题的能力,由关系图确定产生氢气的质量是正确解答本题的关键.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
下列物质可以用于干燥CO2气体的是( )
| A、炭粉 | B、浓硫酸 |
| C、氢氧化钠 | D、生石灰 |
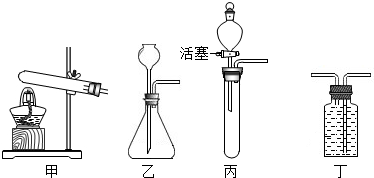 某化学实验小组的同学用如图所示装置进行制备气体的探究.
某化学实验小组的同学用如图所示装置进行制备气体的探究.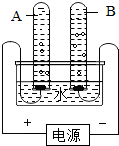 水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题:
水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题: (1)最初输水管材用铸铁,目前多用塑料管,输送热水一般用铜管.
(1)最初输水管材用铸铁,目前多用塑料管,输送热水一般用铜管.


