题目内容
1.木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如图:
(1)写出反应①的化学方程式H2SO4+CuO═CuSO4+H2O:
(2)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入烧杯中(填仪器名称),然后用玻璃棒不断搅拌(填操作名称),使反应充分进行.
(3)试剂A可选用H2SO4溶液(填一种物质的化学式).
(4)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)回收滤渣I中的Cu.
分析 (1)根据反应流程及反应物和生成物写出化学方程式;
(2)根据烧杯可用作较多试剂进行反应的容器进行解答;
(3)根据要除去铜粉中的铁粉,可加入稀硫酸进行解答;
(4)要得到更多的铜,可将反应过程中的铜回收或再利用.
解答 解:(1)反应①氧化铜与硫酸反应生成硫酸铜和水(铜、木炭与硫酸不反应),化学方程式为:H2SO4+CuO═CuSO4+H2O;
(2)较多量试剂的反应容器可在烧杯中,为了加快反应速率可用玻璃棒不断搅拌;
(3)滤渣Ⅱ中含有剩余的铁粉,铁和硫酸反应生成硫酸亚铁和氢气,而铜不和硫酸反应,因此可加入硫酸除去铁;
(4)开始混合粉末中的铜没有和酸反应,进入滤渣Ⅰ中,为了回收更多的铜,可将滤渣Ⅰ中的铜也回收,或将滤渣I在空气中充分灼烧,再投入反应①中.
答案:
(1)H2SO4+CuO═CuSO4+H2O;
(2)烧杯; 用玻璃棒不断搅拌;
(3)H2SO4;
(4)回收滤渣I中的Cu.
点评 对于流程图的题目关健是看明白流程图中各物质的转化关系,注意过量物质的去向,如何除去过量物质.

练习册系列答案
相关题目
9.某化学兴趣小组探究采用下列花汁,制作酸碱指示剂,实验记录如下:
根据以上信息回答:
(1)小明用此月季花的花汁,检测附近造纸厂排放废水的酸碱性,溶液呈浅红色,则此废水显酸性.
(2)小芳用此玫瑰花的花汁,检测家中花盆土壤的酸碱性,溶液呈绿色,则此花盆的土壤显碱性.
(3)小军已检验出纯碱溶液显碱性,他不可能选择的花汁是万寿菊.
| 鲜花汁 | 在稀盐酸中 | 在氯化钠溶液中 | 在氢氧化钠溶液中 |
| 红玫瑰 | 粉红色 | 粉红色 | 绿色 |
| 月季花 | 浅红色 | 红色 | 黄色 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
(1)小明用此月季花的花汁,检测附近造纸厂排放废水的酸碱性,溶液呈浅红色,则此废水显酸性.
(2)小芳用此玫瑰花的花汁,检测家中花盆土壤的酸碱性,溶液呈绿色,则此花盆的土壤显碱性.
(3)小军已检验出纯碱溶液显碱性,他不可能选择的花汁是万寿菊.
6.下列性质中,与二氧化碳灭火无关的是( )
| A. | 它能溶于水 | B. | 一般情况下,它不能燃烧 | ||
| C. | 它的密度比空气大 | D. | 一般情况下,它不支持燃烧 |
 人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此死亡.如图所示为“维生素C”说明书的一部分.请你回答:
人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此死亡.如图所示为“维生素C”说明书的一部分.请你回答: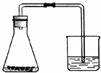 如图,向锥形瓶中加入饱和食盐水,润湿铁丝,塞紧带导管的单口塞,导管的另一端伸入红色的水中,2-3个小时后,观察到导管内红色的水的液面会( )
如图,向锥形瓶中加入饱和食盐水,润湿铁丝,塞紧带导管的单口塞,导管的另一端伸入红色的水中,2-3个小时后,观察到导管内红色的水的液面会( )