题目内容
4.2016年4月15日是我国首个“全民国家安全教育日”.下列说法错误的是( )| A. | 煤矿的矿井要加强通风,防止发生爆炸 | |
| B. | 酒精能破坏蛋白质结构,可用于杀菌消毒 | |
| C. | 厨房天然气泄露,可打开抽油烟机排气 | |
| D. | 进入久未开启的地窖,要做灯火实验 |
分析 A、根据煤矿的矿井可能含有可燃性气体进行解答;
B、根据酒精能使蛋白质变性进行解答;
C、根据天然气属于可燃性气体,遇明火可能会发生爆炸进行解答;
D、根据久未开启的地窖中二氧化碳的含量可能过高,且二氧化碳不燃烧也不支持燃烧进行解答.
解答 解:A、煤矿的矿井可能含有可燃性气体,遇明火可能会发生爆炸,所以煤矿的矿井要加强通风,防止发生爆炸,故A正确;
B、酒精能使蛋白质变性,所以酒精能用于杀菌消毒,故B正确;
C、天然气属于可燃性气体,遇明火可能会发生爆炸,所以厨房天然气泄露,不可打开抽油烟机排气,应该关闭阀门,并且开窗通风,故C错误;
D、久未开启的地窖中二氧化碳的含量可能过高,且二氧化碳不燃烧也不支持燃烧,所以进入久未开启的地窖,要做灯火实验,故D正确.
故选:C.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
14.某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究,
【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】
①15℃、101KPa时,二氧化碳的溶解度如下:
②15℃时,在酒精中氢氧化钠易溶、碳酸钠微溶.
③通常情况下,稀溶液的体积约等于溶剂的体积.
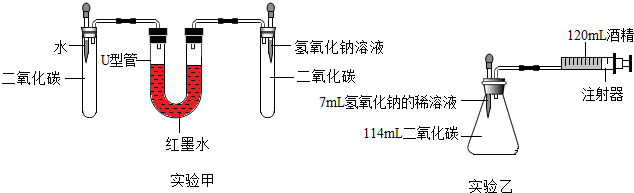
【实验设计】在15℃、101KPa时,制取二氧化碳并用于实验甲、实验乙.
【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是2NaOH+CO2=Na2CO3+H2O,那么氢氧化钠应密封保存.
(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是往U形管内加入适量的水,连接装置,用手捂住一支试管,观察U形管内液面变化,然后用手捂住另一只试管,再次观察U形管内液面变化
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,右侧液面仍高于左侧
(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是B.(填答案字母)
A.先慢后快 B.先快后慢 C.先慢后快,再变慢
实验乙中,还可能观察到的现象是在锥形瓶中观察到白色浑浊现象.
(5)实验乙中,120mL酒精不能(填“能”或“不能”)换成水,原因是二氧化碳在水中的溶解度大于在酒精中,碳酸钠在酒精中微溶,现象明显.
(6)实验乙结束时,注射器中酒精体积为20mL,则与氢氧化钠反应的二氧化碳体积至少是43mL.
(7)由以上探究可知,二氧化碳能溶于水,也能氢氧化钠反应,但实验乙的数据还不够准确,造成实验乙误差的原因可能有酒精具有挥发性.(写一条)
【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】
①15℃、101KPa时,二氧化碳的溶解度如下:
| 溶剂 | 水 | 酒精 |
| 溶解度 | 1.0 | 0.5 |
③通常情况下,稀溶液的体积约等于溶剂的体积.
【实验设计】在15℃、101KPa时,制取二氧化碳并用于实验甲、实验乙.

【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是2NaOH+CO2=Na2CO3+H2O,那么氢氧化钠应密封保存.
(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是往U形管内加入适量的水,连接装置,用手捂住一支试管,观察U形管内液面变化,然后用手捂住另一只试管,再次观察U形管内液面变化
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,右侧液面仍高于左侧
(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是B.(填答案字母)
A.先慢后快 B.先快后慢 C.先慢后快,再变慢
实验乙中,还可能观察到的现象是在锥形瓶中观察到白色浑浊现象.
(5)实验乙中,120mL酒精不能(填“能”或“不能”)换成水,原因是二氧化碳在水中的溶解度大于在酒精中,碳酸钠在酒精中微溶,现象明显.
(6)实验乙结束时,注射器中酒精体积为20mL,则与氢氧化钠反应的二氧化碳体积至少是43mL.
(7)由以上探究可知,二氧化碳能溶于水,也能氢氧化钠反应,但实验乙的数据还不够准确,造成实验乙误差的原因可能有酒精具有挥发性.(写一条)
15.某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是Ⅲ
Ⅰ;CaOⅡ.Ca(OH)2 Ⅲ.CaCO3 Ⅳ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应.
【实验与事实】
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理:CaCO3+2HCl═CaCl2+CO2↑+H2O,Ca(OH)2+CO2═CaCO3↓+H2O;
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是Ⅲ
Ⅰ;CaOⅡ.Ca(OH)2 Ⅲ.CaCO3 Ⅳ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应.
【实验与事实】
| 实验 | 现象 | 解释或结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不变色说明水垢中一定没有Ca(OH)2 |
| 实验二 | 按如图所示方案进行实验 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成,则水垢中一定含有CaCO3 |
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
16.下列利用空气某成分物理性质的是( )
| A. | 氧气可以供给呼吸 | B. | 氮气可以制造化肥 | ||
| C. | 干冰用于人工降雨 | D. | 稀有气体用作保护气 |
13.将50克碳酸钙高温煅烧一段时间,冷却后投入足量的稀盐酸中完全反应.下列说法错误的是( )
| A. | 煅烧越充分则消耗盐酸越少 | |
| B. | 整个反应过程中产生的二氧化碳总质量22克 | |
| C. | 煅烧后固体中氧元素质量分数减小 | |
| D. | 反应结束后共生成55.5克氯化钙 |
18.小林同学在学完中和反应知识后思考,除了通过酚酞变色说明氢氧化钠与稀盐酸能发生反应,还有什么方法能说明两者能反应?小组同学讨论后进行以下实验探究.
方案一:测定氢氧化钠和稀盐酸溶液混合前后的pH.
将一定量的稀盐酸加入pH=13的氢氧化钠溶液中,均匀混合后测定此溶液的pH等于5.
结论:稀盐酸与氢氧化钠溶液发生反应,并且该反应中稀盐酸过量.该反应的化学方程式为NaOH+HCl=NaCl+H2O.
方案二:小林查阅资料得知中和反应都是放热反应.同学们分别进行实验,小林用手触摸发现不同的小组实验放出的热量不同.
【提出问题】影响氢氧化钠溶液与稀盐酸反应放热多少的因素是什么?
【做出猜想】猜想一:反应物的浓度;
猜想二:反应物的用量.
…
【交流讨论】要准确判断放出热量的多少,不能仅凭手触摸,要用温度计测量反应前后的温度,然后再根据一定数据计算得出.
【设计实验】为验证猜想,同学们设计了如下实验.(溶液初始温度均为20℃)
【反思质疑】小涛同学通过测定氢氧化钠固体与稀盐酸混合前后温度变化,证明两者发生了反应.小组同学一致认为该方案不合理,理由是氢氧化钠固体溶于水会放出热量使温度升高.
方案一:测定氢氧化钠和稀盐酸溶液混合前后的pH.
将一定量的稀盐酸加入pH=13的氢氧化钠溶液中,均匀混合后测定此溶液的pH等于5.
结论:稀盐酸与氢氧化钠溶液发生反应,并且该反应中稀盐酸过量.该反应的化学方程式为NaOH+HCl=NaCl+H2O.
方案二:小林查阅资料得知中和反应都是放热反应.同学们分别进行实验,小林用手触摸发现不同的小组实验放出的热量不同.
【提出问题】影响氢氧化钠溶液与稀盐酸反应放热多少的因素是什么?
【做出猜想】猜想一:反应物的浓度;
猜想二:反应物的用量.
…
【交流讨论】要准确判断放出热量的多少,不能仅凭手触摸,要用温度计测量反应前后的温度,然后再根据一定数据计算得出.
【设计实验】为验证猜想,同学们设计了如下实验.(溶液初始温度均为20℃)
| 实验编号 | 氢氧化钠溶液的用量及质量分数 | 稀盐酸的用量 及质量分数 | 比较充分反应后溶液温度 | 实验 结论 |
| 1 | 10mL10% | 20mL10% | 实验1的温度>实验2的温度. (填“>”或“<”) | 猜想一 正确 |
| 2 | 10mL5% | 20mL10% |
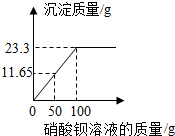 某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析: