题目内容
12.除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | CaO固体 | CaCO3固体 | 加入适量的稀盐酸 | 过滤、洗涤、干燥 |
| B | H2 | 水蒸气 | 适量的NaOH溶液 | 洗气 |
| C | 硝酸 | 盐酸 | 过量的硝酸银溶液 | 过滤 |
| D | BaCl2 | HCl | 过量BaCO3 | 溶解、过滤 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CaO固体和CaCO3固体均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、NaOH溶液不具有吸水性,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、盐酸能与过量的硝酸银反应生成氯化银沉淀和硝酸,能除去杂质但引入了新的杂质硝酸银(过量的),不符合除杂原则,故选项所采取的方法错误.
D、HCl能与过量BaCO3反应生成氯化钡、水和二氧化碳,再过滤除去过量的难溶于水的碳酸钡,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
2.物质X是一种可再生绿色能源,其燃烧的化学方程式为X+302$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,则X的化学式为( )
| A. | C2H4 | B. | CH3OH | C. | C2H5OH | D. | C2H6 |
7.草莓、香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2)等物质.下列关于乙酸乙酯的说法正确的是( )
| A. | 该物质是由4个碳元素、8个氢元素和2个氧元素组成的 | |
| B. | 1个乙酸乙酯分子中含有4个水分子 | |
| C. | 乙酸乙酯中碳、氢、氧的质量比为2:4:1 | |
| D. | 乙酸乙酯中各元素的质量分数比较:C%>O%>H% |
17.下列各组物质在pH=1的无色溶液中,能大量共存的是( )
| A. | CuCl2,NaCl,K2SO4 | B. | KCl,Na2CO3,NaNO3 | ||
| C. | NaOH,Na2SO4,KCl | D. | KNO3,H2SO4,NaCl |
2.下列物质充分反应后所得溶液质量比反应前总质量减小的是( )
| A. | 氧化铁加入稀盐酸中 | B. | 硫酸铜溶液和氯化钡溶液混合 | ||
| C. | 氢氧化钠溶液和稀硫酸混合 | D. | 三氧化硫通入氢氧化钠溶液中 |


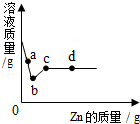 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.