题目内容
4.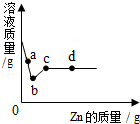 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.(1)请写出a点所发生反应的化学方程式.
(2)c点所示的溶液中含有哪些溶质?
(3)d点表示的固体中含有哪些物质?
分析 根据已有的金属活动性顺序的意义进行分析解答,锌比铜和银活泼,锌能和硝酸银反应生成硝酸锌和银,能和硝酸溶反应生成硝酸锌和铜,据此解答.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程;
(1)锌首先能和硝酸银反应生成硝酸锌和银,故a点是锌和硝酸银的反应,故答案为:Zn+2AgNO3=Zn(NO3)2+2Ag;
(2)c点时硝酸铜和硝酸银都全部反应,故c点的溶质只有硝酸锌,故答案为:Zn(NO3)2;
(3)d点时锌过量,含有的金属是锌、铜和银,故答案为:锌、铜、银.
点评 本题考查的是金属活动性顺序的应用,完成此题,可以依据已有的金属活动性顺序的意义进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列实验方法不正确的是( )
| A. | 用二氧化锰区分水和5%过氧化氢溶液 | |
| B. | 用燃着的木条区分氮气和二氧化碳气体 | |
| C. | 用适量的稀硫酸除去木炭粉中混有的少量氧化铜 | |
| D. | 用适量的铁粉除去氯化亚铁溶液中混有的少量氯化锌 |
15.下列物质的转化,不能一步实现的是( )
| A. | H2O→H2 | B. | Fe→FeCl3 | C. | Cu(OH)2→CuCl2 | D. | C→CO |
12.除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )
| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | CaO固体 | CaCO3固体 | 加入适量的稀盐酸 | 过滤、洗涤、干燥 |
| B | H2 | 水蒸气 | 适量的NaOH溶液 | 洗气 |
| C | 硝酸 | 盐酸 | 过量的硝酸银溶液 | 过滤 |
| D | BaCl2 | HCl | 过量BaCO3 | 溶解、过滤 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
9.2014 年诺贝尔化学奖被美德两国科学家共同获得,其获奖理由是:发展了超高分辨率荧光显微镜.通过他们的贡献,科学家可以在细胞中观察到单个蛋白质分子的运动.下列说法不正确的是( )
| A. | 分子是真实存在的 | |
| B. | 分子总是不断运动的 | |
| C. | 不同蛋白质分子混合一起后是混合物 | |
| D. | 甲醛不会破坏蛋白质的结构 |
16.下列物质在氧气中燃烧发出耀眼白光的是( )
| A. | 白磷 | B. | 铁丝 | C. | 硫磺 | D. | 镁条 |
13.如图显示了x、y、z三种液体的近似pH,下列判断不正确的是( )


| A. | z显碱性 | B. | y一定是水 | ||
| C. | x可能是硫酸溶液 | D. | z 可使紫色石蕊试液变蓝 |
14.镁元素的原子结构示意图为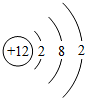 ,下列说法错误的是( )
,下列说法错误的是( )
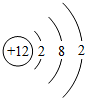 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 镁元素属于金属元素 | B. | Mg2+最外层有2个电子 | ||
| C. | 镁元素原子核内的质子数为12 | D. | 镁原子在化学反应中容易失去电子 |