题目内容
6.为测定一瓶氢氧化钠溶液的质量分数,小张同学进行了以下实验:如图1所示,在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止.

请回答:
(1)酚酞溶液的作用是判断氢氧化钠与盐酸恰好完全反应.
(2)当溶液颜色恰好变为无色时,共用去稀盐酸7.3g,则该氢氧化钠溶液中溶质的质量分数为1.6%.
(3)在以上实验操作中,如继续滴加1%稀盐酸,并不断搅拌,则整个实验过程中溶液pH的
变化曲线如图2所示.
①a点表示的含义是恰好中和;
②b点溶液中含有的阳离子有Na+、H+(填离子符号).
(4)图3是盐酸滴入氢氧化钠溶液中有关粒子之间反应的示意图.由此可看出,盐酸与氢氧化钠能发生反应的原因是氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子反应生成水分子.
分析 (1)根据酚酞遇碱性溶液变红,可以用来检验酸碱是否发生中和反应;
(2)根据氢氧化钠与盐酸的反应,由盐酸溶质的质量求出氢氧化钠的质量,再求出氢氧化钠溶液中溶质的质量分数;
(3)根据溶液pH的变化图象的意义,分析a的含义、b点溶液中的阳离子;
(4)氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子反应生成水分子.
解答 解:(1)酚酞遇碱性溶液变红,酚酞溶液的作用是:判断反应是否恰好完成;
(2)盐酸中溶质的质量为:7.3g×1%=0.073g
设氢氧化钠的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.073g
$\frac{40}{36.5}=\frac{x}{0.073g}$
解得:x=0.08g
甲组这瓶氢氧化钠溶液中溶质的质量分数为:$\frac{0.08g}{5g}×100%$=1.6%;
(3)①由溶液pH的变化图象可知,在a点时,溶液的pH等于7,说明了氢氧化钠和盐酸恰好中和;②在b点时,溶液呈酸性,氢氧化钠全部与盐酸反应生成了氯化钠,溶液中还有剩余的盐酸.所以溶液中的阳离子是:Na+、H+;
(4)盐酸与氢氧化钠能发生反应的原因是氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子反应生成水分子.
答案:(1)判断氢氧化钠与盐酸恰好完全反应;
(2)1.6%;
(3)①恰好中和 (或溶液呈中性,或溶液的pH=7);②Na+、H+;
(4)氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子反应生成水分子(或有水生成).
点评 本题是考查中和反应过程中溶液pH的变化情况的,我们要知道向酸中加碱和向碱中加酸时,溶液pH的变化趋向.明确不同指示剂的变色范围.

练习册系列答案
相关题目
16.鉴别NaOH和Ca(OH)2溶液,应选用的物质是( )
| A. | 紫色的石蕊试液 | B. | 无色的酚酞试液 | C. | CO2气体 | D. | 稀盐酸 |
17.下列物质露置在潮湿的空气中一段时间后,质量不会增加的是( )
| A. | 浓硫酸 | B. | 铁粉 | C. | 烧碱 | D. | 浓盐酸 |
14.为研究NaOH与盐酸的反应,同学们用以下试剂设计不同方案进行探究.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出,乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
查阅资料:
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出,乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
| 实验序号 | A | B | C | D |
| 试剂 | 蒸馏水 | 稀盐酸 | NaOH溶液 | NaCl溶液 |
| 电流强度/mA | 约为0 | 0.09 | 0.09 | 0.09 |
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
11.下列日常学习生活中的做法正确的是( )
| A. | 坚持只喝纯净水 | B. | 把浓硫酸倒入盛有水的量筒里稀释 | ||
| C. | 进入深洞时要带电筒还要打火把 | D. | 用亚硝酸钠代替食盐作调味品 |
15.甲、乙两化学兴趣小组用如图1所示的实验装置,通过测定产生相同体积氧气所用时间的长短来探究影响H2O2分解速率的因素.
(1)甲组:按如下设计的方案实验,请完成表1:
(2)乙组:按如下设计的方案实验,请完成表2:
(3)甲、乙两小组通过数次实验得出如图2所示的数据,请回答下列问题: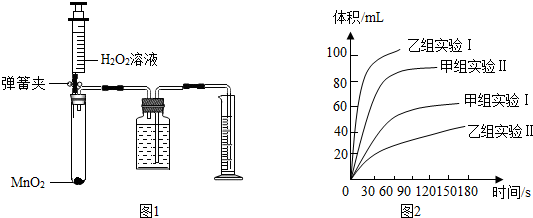
①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
(1)甲组:按如下设计的方案实验,请完成表1:
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| Ⅰ | 探究溶液的浓度对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 10mL 4%H2O2 |
| Ⅱ | 25℃ | 0.2gMnO2 | 10mL 8%H2O2 |
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 实验时溶液 酸碱度 |
| Ⅰ | 探究溶液的酸碱性 对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 0mL 8%H2O2 | pH=10.0 |
| Ⅱ | 25℃ | 0.2gMnO2 | 0mL 8%O2 | pH=4.0 |

①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.