��Ŀ����
5�������е����ĺ�����࣬�����ڸ��¡������������¿���ijЩ���ʷ�����Ӧ����ͼ���Կ�����������Ҫ��ԭ�Ϻϳɵ��ʣ�NH4NO3���Ĺ�ҵ���̣��밴Ҫ��ش�����������1��д��������з�����Ӧ�Ļ�ѧ����ʽ4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
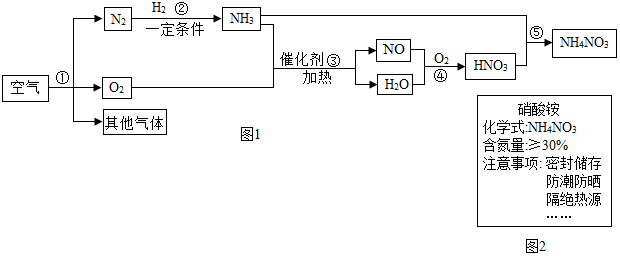
��2��������ѧ��Ӧ�����ڻ��Ϸ�Ӧ����3����
��3����ͼ2�ǻ�������藺�װ���ϵIJ���˵���������Ӧ���е�������A������ĸ��
A��������ˮ B���лӷ��� C�������ֽ�
ʩ�ø������ʱ��Ҫ������������ʻ��ʹ�ã�д�����������ʯ�ҷ�Ӧ�Ļ�ѧ����ʽ2NH4NO3+Ca��OH��2=Ca��NO3��2+2H2O+2NH3����
���� ���ݸ�����ת����ϵ��Ӧ�Ĺ��̷���ÿ����Ӧ�����⣬����ֱ�ӷ���ÿ�����⣬�Ӹ�������Ϣ���Ҷ�Ӧ����Ϣ��
��� �⣺
��1��������ǰ����������ڴ����ͼ�������������NO��ˮ����Ӧ�Ļ�ѧ����ʽ 4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��2�����������д�ǰ�����漰���Ļ�ѧ��Ӧ����ΪN2+3H2$\frac{\underline{\;һ������\;}}{\;}$2NH3�����һ��Ϊ���Ϸ�Ӧ����4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O�������ڻ�����Ӧ���ͣ���4NO+3O2+2H2O=4HNO3�����һ��Ϊ���Ϸ�Ӧ����NH3+HNO3=NH4NO3�����һ��Ϊ���Ϸ�Ӧ��������������ѧ��Ӧ�����ڻ��Ϸ�Ӧ���� 3����
��3����������藺�װ���ϵIJ���˵����������ʾ�ܷⱣ�棬������������������ˮ��
ʩ�ø������ʱ��Ҫ������������ʻ��ʹ�ã�����Ϊ�̬�����������������ܹ���Ӧ���ɰ�������ɷ�Ч���ͣ����������ʯ�ҷ�Ӧ��������ƺ�ˮ�Լ���������Ӧ�Ļ�ѧ����ʽ 2NH4NO3+Ca��OH��2=Ca��NO3��2+2H2O+2NH3����
�ʴ�Ϊ��
��1��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��2��3��
��3��A�� 2NH4NO3+Ca��OH��2=Ca��NO3��2+2H2O+2NH3����
���� ��ͼ�����л�ý����Ŀ�������Ϣ�������ڽ����Ŀʱ�ȿ�����������ʲô��Ȼ���������ȥ��������ͼ����ȥѰ�ҽ�����õ���Ϣ�������������Ϣ������Ч�ԣ���������ʵ�����븴�ӵ�ת��ͼ��ȣ���ʵ�ܼܻ��������߿���˵ת��ͼ�ṩ�����龳���������֪ʶ��

| A�� | ȼ����Ҫ��ȼ��Ӵ����������Կ�ȼ��Ӵ�������һ����ȼ�� | |
| B�� | ��ϴ���ϴȥ�������������黯���ã�������ϴȥ����Ҳ���������黯���� | |
| C�� | ��Һ���о�һ���ȶ������������Ծ�һ���ȶ���Һ��һ������Һ | |
| D�� | ����ϡ���ᷴӦ����Һ��������п��ϡ���ᷴӦ����Һ����Ҳ���� |
| A�� | ���ڿ�����ȼ�գ���������ɫ���棬�����д̼�����ζ������ | |
| B�� | ��˿��������ȼ�գ��������䣬�ų����������ɺ�ɫ���� | |
| C�� | �����ڿ�����ȼ�ղ��������İ��� | |
| D�� | ������������ȼ�ղ��������İ��� |

| A�� | �ס��ҡ��ס������ס��� | B�� | �ס������ҡ��ס��� | ||
| C�� | �ס��ҡ������ҡ��� | D�� | �ҡ��ס������ס��� |
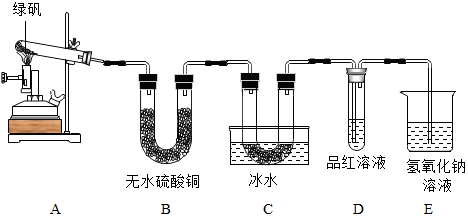

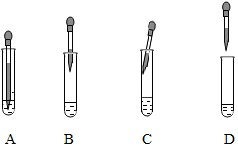


 A��B��C��D��E�dz��л�ѧ���������ʣ�CΪ���ʣ�������B ��D����������� E�㷺���ڲ�������ֽ����֯��ϴ�Ӽ�������������֮���һ���ֹ�ϵ��ͼ��ʾ����ͼ�С�-����ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ���ʼ����ת����ϵ�����ַ�Ӧ�������������ȥ��
A��B��C��D��E�dz��л�ѧ���������ʣ�CΪ���ʣ�������B ��D����������� E�㷺���ڲ�������ֽ����֯��ϴ�Ӽ�������������֮���һ���ֹ�ϵ��ͼ��ʾ����ͼ�С�-����ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ���ʼ����ת����ϵ�����ַ�Ӧ�������������ȥ��