题目内容
15.某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空.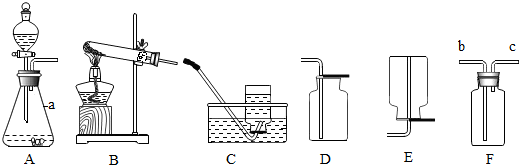
(1)写出仪器a的名称锥形瓶.
(2)实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.若用F进行排空法收集二氧化碳,则气体应从b口进入(填b或c).
(3)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的一套装置是BC.
分析 (1)根据常见的化学仪器的名称,进行分析解答.
(2)实验室制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,结合二氧化碳的密度比空气的大,进行分析解答.
(3)根据实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,甲烷是一种无色、无味、难溶于水的气体,进行分析解答.
解答 解:(1)仪器a的名称是锥形瓶.
(2)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
二氧化碳的密度比空气的大,若用F进行排空法收集二氧化碳,则气体应从b口进入,将空气从a端排出.
(3)实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,属于固体加热型,应该选用的发生装置是B;甲烷是一种无色、无味、难溶于水的气体,可选用排水法收集,即选用C装置收集.
故答案为:(1)锥形瓶;(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;b;(3)BC.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
相关题目
6.鸡蛋壳的主要成分是碳酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,兴趣小组的同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取20g放在烧杯里,然后分4次向烧杯中加入等质量稀盐酸,实验数据如表所示(假设其他物质捕鱼盐酸反应):
根据实验数据回答问题:
(1)表中数据值M=213.4;
(2)完全反应后产生二氧化碳的质量为6.6;
(3)计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程).
| 数据 | 实验1 | 实验2 | 实验3 | 实验4 | 实验5 |
| 加入稀盐酸的质量/g | 0 | 50 | 50 | 50 | 50 |
| 烧杯与烧杯中物质的总质量/g | 70.00 | 117.5 | 165.0 | M | 263.4 |
(1)表中数据值M=213.4;
(2)完全反应后产生二氧化碳的质量为6.6;
(3)计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程).
3.2016年3月22日是第二十四届“世界水日”,宣传主题是“水与就业”.下列跟水有关的变化中没有化学变化的是( )
| A. | 海水晒盐 | B. | 太阳能光解水制氢气 | ||
| C. | 饮用水生产 | D. | 肥老水区分硬水和软水 |
20.PM2.5是指大气中直径大于或等于2.5um的颗粒物.为实现空气质量达标,合理的做法( )
| A. | 煤炭直接燃烧 | B. | 桔杆焚烧还田 | C. | 开发清洁能源 | D. | 提倡多开汽车 |
5.将一定容器中,质量的a、b、c、d四种物质放入一密闭在一定条件下反应段时间后,测得反应后各物质的质量如下:
下列说法错误的是( )
| 物 质 | a | b | c | d |
| 反应前质量/g | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量/g | 待测 | 2.56 | 7.2 | 0.5 |
| A. | a和b是反应物,d可能是催化剂 | |
| B. | 反应后a的质量为2.56g | |
| C. | c物中元素的种类,一定等于a、b、两种物质中元素的种类 | |
| D. | 若a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为1:2 |

 人体缺乏维生素C(简写Vc)就会患坏血病.如图为某种“维生素C”说明书的一部分,请回答:
人体缺乏维生素C(简写Vc)就会患坏血病.如图为某种“维生素C”说明书的一部分,请回答: