题目内容
20.PM2.5是指大气中直径大于或等于2.5um的颗粒物.为实现空气质量达标,合理的做法( )| A. | 煤炭直接燃烧 | B. | 桔杆焚烧还田 | C. | 开发清洁能源 | D. | 提倡多开汽车 |
分析 根据PM2.5是指大气中直径小于或等于2.5微米的颗粒物分析.
解答 解:A、煤炭直接燃烧产生大量的二氧化硫、氮氧化物、一氧化碳及烟尘等空气污染物,故A不合理;
B、在露天焚烧秸秆可以产生烟尘,直接进入大气,会增加空气中PM2.5,故B不合理;
C、清洁能具有无污染性,不会增加空气中PM2.5,故C合理;
D、汽车排放尾气中含有一些烟尘,进入大气,会增加空气中PM2.5,故D不合理;
故填:C.
点评 环境的污染与保护是社会关注的焦点问题,与之相关的考题就成为中考的热点之一.解答本题关键是看是否减少了对空气中可吸收颗粒物的释放.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
8.90g镁、铁、锌的混合物与足量的稀硫酸反应得到混合液,蒸发得到378g硫酸盐固体,则反应生成的氢气质量为( )
| A. | 4.0g | B. | 4.8g | C. | 5.6g | D. | 6.Og |
12.下列有关水的说法中正确的是( )
| A. | 硬水和软水可以用石蕊试液来区分 | |
| B. | 常用吸附、沉淀、过滤、蒸馏等方法净化水 | |
| C. | 水变成水蒸气时体积增大是因为水分子体积变大 | |
| D. | 所有溶液中的溶剂均为水 |
9. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )| A. | 40℃时,50g甲的饱和溶液中溶解了25g的甲 | |
| B. | 将20℃时甲、乙两种物质的饱和溶液升温至40℃(溶剂的量不变),两种溶液中溶质的质量分数相等 | |
| C. | 20℃时,使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法 | |
| D. | 40℃时,将质量都为40g的甲、乙两种物质的饱和溶液降温至20℃,析出甲的质量比析出乙的质量大 |
10.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出)

【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水、和氮气.
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
(3)本实验条件下,氮气密度为1.15g•L-1.装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)取一定量氧化铜,准确称得其质量为2.40g.
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表1)
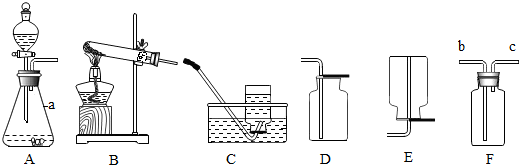
【实验装置】如图2
【相关数据】
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
(4)通过计算推导出气体X的化学式为NH3.气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.

【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水、和氮气.
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
(3)本实验条件下,氮气密度为1.15g•L-1.装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)取一定量氧化铜,准确称得其质量为2.40g.
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表1)
【实验装置】如图2
【相关数据】
| 数据编号 测量项目 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | / | 243.5 |
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
(4)通过计算推导出气体X的化学式为NH3.气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
 2014年3月8日凌晨,马来西亚航空公司一架载有239人(其中154名中国人)的客机在飞往北京的途中突然失踪,引起全世界的关注,多个国家参与搜索,其中飞机“黑匣子”(名为航空飞行记录器)是搜寻的重点之一.制取“黑匣子”的材料之一是金属钛,钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3.请回答:
2014年3月8日凌晨,马来西亚航空公司一架载有239人(其中154名中国人)的客机在飞往北京的途中突然失踪,引起全世界的关注,多个国家参与搜索,其中飞机“黑匣子”(名为航空飞行记录器)是搜寻的重点之一.制取“黑匣子”的材料之一是金属钛,钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3.请回答: