题目内容
10.我国新修订的《环境保护法》已于2015年1月1日起施行,体现了加强生态文明建设的新要求.(1)①近期许多城市出现雾霾天气,形成雾霾是空气中PM2.5含量的增加.PM2.5指的是d
a.SO2b.CO c.NO2 d.可吸入颗粒物
②治理被酸雨侵蚀的酸性土壤,可加入适量的b(填字母).
a.KCl b.Ca(OH)2 c.SiO2
(2)目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和天然气,该物质主要成分燃烧的化学方程式是CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)二氧化氯(ClO2)是新一代饮用水的消毒剂,工业上将氯气(Cl2)通入亚氯酸钠(NaClO2)溶液中反应来制取二氧化氯,同时生成氯化钠.写出该反应的化学方程式:Cl2+2NaClO2═2NaCl+2ClO2.
分析 (1)①从PM2.5指细颗粒物,细颗粒物指环境空气中空气动力学当量直径小于等于 2.5 微米的颗粒物,属于可吸入颗粒物去分析解答;
②熟石灰是氢氧化钙的俗称,为常见的碱,能与酸发生中和反应;
(2)化石燃料包括煤、石油、天然气;天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水;
(3)根据参加反应的物质及生成的物质,完成反应化学方程式的书写.
解答 解:(1)①PM2.5指细颗粒物,细颗粒物指环境空气中空气动力学当量直径小于等于2.5微米的颗粒物;
②熟石灰能与酸性土壤中酸性物质发生反应,可用于改良酸性土壤;
(2)化石燃料包括煤、石油、天然气;天然气的主要成分是甲烷,甲烷燃烧生成二氧化碳和水,反应的方程式是:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)由氯气在溶液中与亚氯酸钠反应生成二氧化氯和氯化钠可知:该化学方程式为Cl2+2NaClO2═2NaCl+2ClO2;
故答案为:(1)①d;②b.
(2)天然气;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)Cl2+2NaClO2═2NaCl+2ClO2.
点评 此题考查的知识点较多,而且较为全面,以一定的难度,需要同学们能够牢靠掌握基础知识.

练习册系列答案
相关题目
1.小强将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后有气泡冒出.他对所产生气体的成分及排水口洗净剂主要成分进行探究.
【探究活动一】
老师提示:排水口洗净剂与水作用的生成物中有两种常见的气体.小强设计并进行如图所示的实验.

实验现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺.由此得出结论:生成的两种气体分别是:二氧化碳和氧气.B中有关反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
【探究活动二】
老师提供了一瓶过碳酸钠( Na2CO4),引导小强进行如下实验探究:

根据上述实验结果得出结论:无色溶液x中含有的一种溶质是过氧化氢.根据质量守恒定律,小强对溶液x中还可能存在其它溶质作出如下猜想:
①Na2CO3 ②NaHCO3 ③Na2CO3和NaHCO3的混合物.
资料摘要I:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2=CaCO3↓+2NaC1
资料摘要Ⅱ:NaHCO3溶液呈碱性;碳酸氢钠、碳酸钠分别与足量的酸反应产物相同.
实验验证:
综合上述两个探究活动的结果,小强明确了上述猜想①(填序号)是正确的.
【探究活动一】
老师提示:排水口洗净剂与水作用的生成物中有两种常见的气体.小强设计并进行如图所示的实验.

实验现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺.由此得出结论:生成的两种气体分别是:二氧化碳和氧气.B中有关反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
【探究活动二】
老师提供了一瓶过碳酸钠( Na2CO4),引导小强进行如下实验探究:

根据上述实验结果得出结论:无色溶液x中含有的一种溶质是过氧化氢.根据质量守恒定律,小强对溶液x中还可能存在其它溶质作出如下猜想:
①Na2CO3 ②NaHCO3 ③Na2CO3和NaHCO3的混合物.
资料摘要I:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2=CaCO3↓+2NaC1
资料摘要Ⅱ:NaHCO3溶液呈碱性;碳酸氢钠、碳酸钠分别与足量的酸反应产物相同.
实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| a、取上述无色溶液X少量于试管中,至不再冒气泡为止,加入足量的氯化钙溶液 | 产生白色沉淀 | 无色溶液X中含有Na2CO3 |
| b、取步骤a所得上层清液少量,滴加稀盐酸 | 没有气泡产生 | 无色溶液X中不含NaHCO3 |
15.下列各组转化中,一定条件下均能一步实现的组合是( )

| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
2.化学实验中,常用到一种多功能装置.请你回答①~④装置在实验中常用的功能.
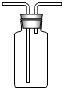 |  ① ① | 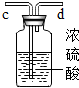 ② ② |  ③ ③ |  ④ ④ |
| 多功能装置 | 可用于收集气体 | 用浓硫酸干燥气体 | 除去二氧化碳中的氯化氢气体 | 收集气体并测量收集的气体的体积 |
20.下列有关酸的性质说法正确的是( )
| A. | 浓盐酸、浓硫酸都能使纸张炭化 | |
| B. | 稀盐酸和稀硫酸都可用于除铁锈 | |
| C. | 浓盐酸、浓硫酸都可用来干燥氧气 | |
| D. | 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾 |
 如图是一种防霾新产品------鼻用空气净化器,它的填充物是硅胶,硅胶可表示为mSiO2•nH2O.
如图是一种防霾新产品------鼻用空气净化器,它的填充物是硅胶,硅胶可表示为mSiO2•nH2O. 为研究溶液中的化学反应对其导电性和浮力的影响,某同学设计了如图所示的实验方案:闭合开关后,灯泡明亮,此时塑料球(密度为1.1g/cm3)漂浮在溶液上,逐渐加入Ba(OH)2溶液直至恰好完全反应,发生反应的化学方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,观察到的现象是灯泡变暗至熄灭,塑料球下沉.
为研究溶液中的化学反应对其导电性和浮力的影响,某同学设计了如图所示的实验方案:闭合开关后,灯泡明亮,此时塑料球(密度为1.1g/cm3)漂浮在溶液上,逐渐加入Ba(OH)2溶液直至恰好完全反应,发生反应的化学方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,观察到的现象是灯泡变暗至熄灭,塑料球下沉.