题目内容
8.同学们从山上采集到一种石灰石,他们取80克该样品加入100克的稀盐酸进行实验(所含杂质不溶于水也不和稀盐酸反应),每隔一段时间测定烧杯内剩余物质质量.测得烧杯内剩余物质的质量(m)与反应时间(t)的关系如下表:| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后物质质量m∕g | 180 | 175 | 170 | 166 | 162 | 158 | 158 |
(1)当石灰石完全反应后,生成CO2的质量为22g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由表格数据分析可知,时间为t5时,烧杯内剩余物质的质量不再改变,说明碳酸钙已完全反应,根据质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳的质量,据此根据反应的化学方程式列式计算出参加反应的碳酸钙的质量,进而计算出该石灰石中CaCO3的质量分数.
解答 解:(1)生成CO2的质量为80g+100g-158g=22g.
(2)设石灰石中CaCO3的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 22g
$\frac{100}{44}=\frac{x}{22g}$ x=50g
石灰石中CaCO3的质量分数为$\frac{50g}{80g}$×100%=62.5%.
答:(1)22;(2)石灰石中CaCO3的质量分数为62.5%.
点评 本题难度不大,掌握利用化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
18.下列实验操作正确的是( )
| A. |  倾倒液体 | B. |  熄灭酒精灯 | C. |  取用固体药品 | D. |  洗涤试管 |

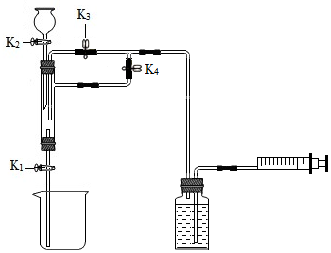 甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:
甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下: