题目内容
12.马明同学完成“细铁丝在氧气中燃烧”的性质实验时对“火星四射”的实验现象产生了兴趣,他在老师的指导下进行了以下实验探究:【提出问题】细铁丝在氧气中燃烧为什么会“火星四射”?
【实验设计】选纯镁条和不同含碳量的铁丝(镁条和铁丝的长度直径相同),放入相同体积的氧气中燃烧作对比试验.
【实验记录】
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧的现象 | 剧烈燃烧,发出耀眼的白光,无火星 | 剧烈燃烧,极少量火星 | 剧烈燃烧,少量火星 | (未记录) |
(2)铁与氧气反应的化学反应方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4:
(3)通过以上探究,你认为铁丝在氧气中燃烧“火星四射”的原因可能是与其含碳量有关,含碳量越高,火星四射越剧烈.
分析 (1)根据题意及表中信息解答;
(2)根据铁丝在氧气中燃烧生成四氧化三铁解答;
(3)根据图中数据可知铁丝燃烧产生火星四射现象和含碳量有关进行解答;
解答 解:
(1)表中“未记录”部分的内容为燃烧比0.2%剧烈,火星四射更明显;故填:剧烈燃烧,大量火星;
(2)铁丝在氧气中燃烧生成四氧化三铁,反应的符号表达式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)根据图中数据可知铁丝燃烧产生火星四射现象和含碳量有关,就铁丝而言,燃烧喷射火星情况与其含碳量的关系为含碳量越高,火星四射越剧烈;故填:与其含碳量有关,含碳量越高,火星四射越剧烈;
答案:
(1)剧烈燃烧,大量火星;
(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)与其含碳量有关,含碳量越高,火星四射越剧烈.
点评 本题考查了学生对于物质的性质、仪器的用途等知识的掌握,同时考查了学生从题目中获取信息,并结合所学知识解答问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列对一些事实的解释不正确的是( )
| 事实 | 解释 | |
| A | 搜救犬搜索到幸存者 | 分子是运动的 |
| B | 双氧水能杀菌消毒而水则不能 | 两种物质的分子构成不同 |
| C | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子很小 |
| D | 加热氧化汞可得到金属汞和氧气 | 分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |
7. 2016年9月在和田地区发现我国境内最大的锌铅矿.铅在元素周期表中的信息如图所示,下列有关铅元素的说法正确的是( )
2016年9月在和田地区发现我国境内最大的锌铅矿.铅在元素周期表中的信息如图所示,下列有关铅元素的说法正确的是( )
 2016年9月在和田地区发现我国境内最大的锌铅矿.铅在元素周期表中的信息如图所示,下列有关铅元素的说法正确的是( )
2016年9月在和田地区发现我国境内最大的锌铅矿.铅在元素周期表中的信息如图所示,下列有关铅元素的说法正确的是( )| A. | 原子序数是82 | B. | 属于非金属元素 | ||
| C. | 原子中的中子数是82 | D. | 相对原子质量为207.2g |
4.下列方法中,相比较得到的水最纯的是( )
| A. | 吸附 | B. | 沉淀 | C. | 过滤 | D. | 蒸馏 |
1.下列实验操作错误的是( )
| A. | 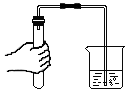 | B. | 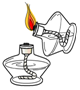 | C. | 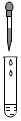 | D. |  |
3.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.近年来科学家发现维生素C有防癌的作用.关于维生素C,下列说法正确的是( )
| A. | 维生素C中C、H、O三种元素的质量比为3:4:3 | |
| B. | 维生素C是氧化物 | |
| C. | 一个维生素C分子由6个碳原子、8个氢原子和6个氧原子构成 | |
| D. | 维生素C是由6个碳元素、8个氢元素和6个氧元素组成 |
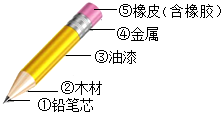 如图是同学们经常使用的铅笔示意图.
如图是同学们经常使用的铅笔示意图. 向某铁粉样品中,加入溶质质量分数为16%的硫酸铜溶液100g,恰好完全反应,样品中杂质不溶于水也不与硫酸铜反应.请结合他提供的数据计算.
向某铁粉样品中,加入溶质质量分数为16%的硫酸铜溶液100g,恰好完全反应,样品中杂质不溶于水也不与硫酸铜反应.请结合他提供的数据计算.