题目内容
7.某无色气体可能含有H2、CO、CH4中的一种或几种,依次进行下列实验(假设每一步反应或吸收均完全)(1)无色气体在氧气中充分燃烧;
(2)将燃烧生成气体通入盛浓硫酸的洗气瓶,洗气瓶的质量明显升高;
(3)再将剩余气体通过盛有澄清石灰水的洗气瓶,出现浑浊现象;
下列说法不正确的是( )
| A. | 该气体一定含有H2、CO、CH4 | B. | 该气体可能含有H2和CO | ||
| C. | 该气体可能含有CO和CH4 | D. | 该气体可能含有CH4 |
分析 根据质量守恒定律和二氧化碳的特性进行解答.
解答 解:无色气体在氧气中充分燃烧,将燃烧生成气体通入盛浓硫酸的洗气瓶,洗气瓶的质量明显升高,说明燃烧生成的气体中含有水,即原混合气体中含有H元素,所以混合气体中含有H2或CH4;
再将剩余气体通过盛有澄清石灰水的洗气瓶,出现浑浊现象,说明燃烧生成的气体中含有CO2,故混合气体中含有C元素.
综上所述,混合气体中可能含有H2和CO,或可能含有CO和CH4,或可能含有CH4,
故选:A.
点评 可燃物完全燃烧时,可燃物中的碳元素全部生成二氧化碳,可燃物中的氢元素全部生成水;可燃物完全燃烧生成二氧化碳和水,可判断可燃物中一定含C、H元素.

练习册系列答案
相关题目
17.对于正在长身体的青少年朋友来说,应加大对富含蛋白质和维生素类的食物摄入,下列食品中富含蛋白质的是( )
| A. | 黄瓜 | B. | 鱼肉 | C. | 果汁 | D. | 馒头 |
18.下列关于物质的性质或变化叙述正确的是( )
| A. | 活性炭净水--化学性质 | |
| B. | 盐酸使石蕊溶液变红--物理性质 | |
| C. | 冰川融化--物理变化 | |
| D. | 工业上分离液态空气制取氧气、氮气--化学变化 |
16.对下列化学用语中数字“2”的说法正确的是( )
①2O3 ②2N ③N2 ④2NO3- ⑤Mg2+ ⑥$\stackrel{+2}{Zn}$SO4 ⑦H2O.
①2O3 ②2N ③N2 ④2NO3- ⑤Mg2+ ⑥$\stackrel{+2}{Zn}$SO4 ⑦H2O.
| A. | 表示离子个数的是④⑤ | B. | 表示离子所带电荷数的是⑤⑥ | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示分子个数的是①② |
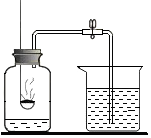 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格. (1)实验中生成沉淀的质量为10g;
(1)实验中生成沉淀的质量为10g;