题目内容
11.下列关于碳和碳的氧化物的说法中,不正确的是( )| A. | 将CO2通入CaCl2溶液中,有白色沉淀生成 | |
| B. | 金刚石、石墨和C60都是碳元素的单质 | |
| C. | 在一定条件下CO2能够转变成CO | |
| D. | 将CO2通入紫色石蕊溶液中,可看到溶液变红 |
分析 根据碳和碳的氧化物的组成、性质和用途等分析判断有关的说法.
解答 解:A、将CO2通入CaCl2溶液中,不会发生反应,没有白色沉淀生成,故A错误;
B、金刚石、石墨和C60都是碳元素的单质,故B正确;
C、在一定条件下CO2能够转变成CO,故C正确;
D、由于二氧化碳能与水化合生成了碳酸,将CO2通入紫色石蕊溶液中,可看到溶液变红,故D正确.
故选A.
点评 根据的难度不大,了解碳和碳的氧化物得得组成和性质、用途等知识即可分析解答.

练习册系列答案
相关题目
1.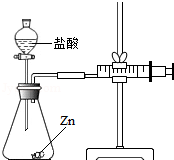 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】
a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同尝试和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑.
从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积.所用药品,实验数据如下表:
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是其他条件相同时,盐酸浓度越大,反应越剧烈.
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).
【拓展延伸】很多金属不仅能与酸反应,也能与盐溶液反应,现将ag铁钉投入到CuSO4溶液中,反应一段时间后,将固体取出洗净、烘干,称重为bg,则生成铜的质量为8(b-a)g.
 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】
a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同尝试和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑.
从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积.所用药品,实验数据如下表:
| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).
【拓展延伸】很多金属不仅能与酸反应,也能与盐溶液反应,现将ag铁钉投入到CuSO4溶液中,反应一段时间后,将固体取出洗净、烘干,称重为bg,则生成铜的质量为8(b-a)g.
19.乙醇(C2H5OH)是可再生能源,其燃烧的化学方程式为C2H5OH+XO2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,试推算X的数值为
( )
( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
16.如表实验操作、现象与结论均正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 用拇指堵住收集了甲烷的试管口,靠近火焰,移开拇指点火 | 发出轻微爆鸣声 | 试管中气体为纯净物 |
| B | 往装有某溶液的试管中滴加稀硫酸 | 产生白色沉淀 | 一定含有Ba2+ |
| C | 把燃着的木条插入某瓶无色气体中 | 木条熄灭 | 该瓶中气体不一定是二氧化碳 |
| D | 在燃烧匙里放少量硫,加热,直到发生燃烧,然后把它伸进充满氧气的集气瓶中 | 硫在空气中燃烧发出淡蓝色火焰,而在氧气中燃烧更旺,发出蓝紫色火焰 | 氧气的浓度越小,燃烧越 |
| A. | A | B. | B | C. | C | D. | D |
3. 某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.
某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.
(1)根据上述信息判断,该无色溶液不可能是HNO3溶液和Fe(NO3)2溶液,只可能是其他3种溶液中的一种.
(2)为了进一步确定该溶液是何种溶液,请你设计实验方案,叙述实验操作、预期现象与结论.限用试剂:稀H2SO4、NaOH溶液、Na2CO3溶液、酚酞溶液、稀盐酸
 某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.
某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Al(NO3)3溶液、Ba(NO3)2溶液、Fe(NO3)2溶液、AgNO3溶液.(1)根据上述信息判断,该无色溶液不可能是HNO3溶液和Fe(NO3)2溶液,只可能是其他3种溶液中的一种.
(2)为了进一步确定该溶液是何种溶液,请你设计实验方案,叙述实验操作、预期现象与结论.限用试剂:稀H2SO4、NaOH溶液、Na2CO3溶液、酚酞溶液、稀盐酸
| 实验操作 | 预期现象与结论 |
| 1 | 实验现象:溶液变浑浊; 实验结论:是硝酸银溶液 |
| 2 | 实验现象:产生白色沉淀; 实验结论:是硝酸钡溶液 |
20.在含有大量Na+、H+、SO42-的溶液中,还可能大量存在的是( )
| A. | OH- | B. | Ba2+ | C. | K+ | D. | CO32- |


 一氧化碳不仅可作燃料,还能作化工原料:
一氧化碳不仅可作燃料,还能作化工原料: